
金属的腐蚀除化学腐蚀和普通的电化学腐蚀外,还有“氧浓差腐蚀”,如在管道或缝隙等处的不同部位氧的浓度不同,在氧浓度低的部位是原电池的负极。下列说法正确的是
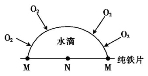
A.纯铁的腐蚀属于电化学腐蚀
B.钢铁吸氧腐蚀时,负极的电极反应式为Fe﹣3e﹣=Fe3﹢
C.海轮在浸水部位镶一些铜锭可起到抗腐蚀作用
D.在图示氧浓差腐蚀中,M极处发生的电极反应为O2+2H2O+4e﹣=4OH﹣
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源:2015-2016河北石家庄第一中学高二上期中考试化学试卷(解析版) 题型:填空题
金刚烷是一种重要的化工原料,工业上可通过下列途径制备:
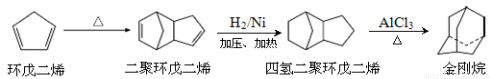
(1)环戊二烯分子中最多有 个原子共平面;
(2)二聚环戊二烯的分子式为 ,金刚烷分子中的-CH2-基团有 个;
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
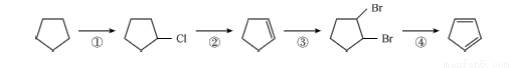
其中,反应③的化学方程式 ,反应④的反应类型是 ;
查看答案和解析>>
科目:高中化学 来源:2016届湖南省株洲市高三上学期期中化学试卷(解析版) 题型:选择题
700 ℃时,向容积为2 L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g) CO2(g)+H2(g)。反应过程中测定的部分数据见下表(表中t2>t1):
CO2(g)+H2(g)。反应过程中测定的部分数据见下表(表中t2>t1):
反应时间/min | n(CO)/mol | H2O/mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
下列说法正确的是( )
A.反应在t1 min内的平均速率为v(H2)= mol·L-1·min-1
mol·L-1·min-1
B.保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2O,到达平衡时n(CO2)=0.30 mol
C.保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大
D.温度升高至800 ℃, 上述反应平衡常数为0.64,则正反应为吸热反应
上述反应平衡常数为0.64,则正反应为吸热反应
查看答案和解析>>
科目:高中化学 来源:2016届湖南长沙市三上学期第四次月考化学试卷(解析版) 题型:简答题
(1)常温下,用0.1000mol·L-1NaOH溶液滴定20.00mL0.100 0mol·L-1CH3COOH溶液所得滴定曲线如下图。已知起始①点溶液的pH为3,③点溶液的pH为7,则Ka(CH3COOH)=____________。

(2)在用Na2SO3溶液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
pH | 8.2 | 7.2 | 6.2 |
0.01mol·L-1Na2SO3溶液中通人SO2至溶液呈中性时,溶液中的所有离子的浓度由大到小的顺序是___________________。
(3)向0.1mol·L-1的NaHSO3中通人氨气至溶液呈中性时,溶液中的c(H+)、c(OH-)、c(SO32-)、c(Na+)、c(NH4+)这五种离子浓度大小关系是____________________。
(4)已知Ca3(PO4)2、CaHPO4均难溶于水,而Ca(H2PO4)2易溶,在含0.1molCa(OH)2的澄清石灰水中逐滴加入1mol·L-1的H3PO4,请作出生成沉淀的物质的量随H3PO4滴人体积从0开始至200mL的图像。

查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三12月月考化学试卷(解析版) 题型:实验题
现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置
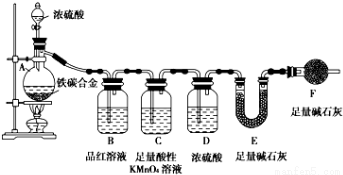
I.探究该合金的某些性质:
(1)取a g合金粉末放人蒸馏烧瓶,并加入足量浓H2SO4,A、B中均无明显现象,原因是_______;
(2)点燃酒精灯一段时间后,A中剧烈反应,请写出此时合金中成分铁的化学反应方程式_____;
(3)反应一段时间后,将C中所吸收的气体通入以下溶液中,判断能否产生沉淀,若不能则写“否”,若能则写出相应的沉淀成分:氯水和氯化钡溶液____,氨水和氯化钡溶液_____;
II.测定样品中碳的质量分数:
(4)装置F的作用__________________________________________________________;
(5)若将SO 2气体通入含有n molNa2S的溶液中,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体_____________mol。
2气体通入含有n molNa2S的溶液中,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体_____________mol。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海西宁第十四中学高一上期中考试化学卷(解析版) 题型:填空题
现有以下物质:①NaCl固体 ②盐酸 ③Ba(OH)2溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体 ⑦乙醇(C2H5OH) ⑧液态硫酸 ⑨熔融态BaSO4 ⑩液态SO3
请回答下列问题(用序号):
以上物质中属于化合物的是____________(填序号,下同),属于盐的是_____________,属于氧化物的是__________,能导电的是___________________,属于电解质的是__________________,属于非电解质的是___________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海西宁第十四中学高二上期中考试化学卷(解析版) 题型:填空题
室温下将pH=13的强碱溶液和pH=2的强酸溶液混合,所得溶液的pH=12,则强碱溶液和强酸溶液的体积之比为 。
查看答案和解析>>
科目:高中化学 来源:2016届辽宁抚顺第一中学高三上第一次模拟考试化学试卷(解析版) 题型:填空题
(1)下列有关说法正确的是_____________。
A.用pH试纸测得新制氯水的pH为4
B.碳酸钠和硫酸钡可按溶解、过滤、蒸发的操作顺序分离
C.除去C2H5OH中的CH3COOH,先加足量的氢氧化钠溶液,再分液
D.溶液中滴加盐酸酸化的BaCl2溶液出现白色沉淀,则该溶液中一定存在SO42-
E.将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中,检验气体中是否含有乙烯
F.用铂丝灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,没有K+
G.金属氧化物不一定是碱性氧化物,但碱性氧化物一定是金属氧化物;非金属氧化物不一定是酸性氧化物,酸性氧化物也不一定是非金属氧化物
H.在两个容积相同的容器中,一盛有HCl气体,另一个盛有H2和Cl2的混合气体,在同温同压下,两容器内的气体一定具有相同的原子数
I.实验室配制1mol/L盐酸250mL,需要的仪器只有:250mL容量瓶、胶头滴管、量筒和烧杯
J.在MH4Al(SO4)2(一种复盐)的溶液中加入Ba(OH)2溶液至沉淀的质量达到最大时:
Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
K.硝酸钡溶液中通入足量的SO2:2SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO↑+4H+
(2)ClO2的制备方法比较实用的有数十种,下列是几种常见的方法.
①方法一:2NaClO3+4HCl(浓)═2NaCl+Cl2↑+2ClO2↑+2H2O
对于该反应,下列说法中正确的是___________。
A.该反应中Cl2是氧化产物
B.该反应中NaCl、ClO2是还原产物
C.在反应中HCl既作氧化剂又具有酸的作用
D.1mol NaClO3参加反应时,有1mol电子发生转移
E.1mol NaClO3参加反应,理论上能得到33.6L气体
方法二:氯化钠电解法
该法工艺原理如图。
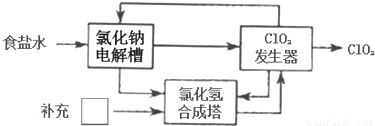
②其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。指出工艺中方框中物质为______(填化学式),理由为______________。
③将NCl3与NaClO2(亚氯酸钠)按物质的量之比1:6混合,在碱性溶液中恰好反应生成ClO2,试写出该反应的离子方程式____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北武汉华中师大一附中高一上期中化学卷(解析版) 题型:实验题
现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
I、 甲同学向1 mol·L-1氯化铁溶液中加入少量的NaOH溶液;
II、 乙同学直接加热饱和FeCl3溶液;
III、 丙同学向25 ml沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是 ;他的操作中涉及到的化学反应方程式为 。
(2)证明有Fe(OH)3胶体生成的实验操作及现象是 。
(3)丁同学将所制得的Fe(OH)3胶体分成两份,并进行下列实验:
①将其中一份装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明 。
②向另一份中不断滴加稀硫酸,观察到的现象是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com