
下列离子方程式,不正确的是
A.用氨水吸收少量二氧化硫:

B.100 mL![]() 的
的![]() 溶液中加入0.01 mol
溶液中加入0.01 mol![]() :
:

C.![]() 的
的![]() 溶液和
溶液和![]() 的盐酸等体积均匀混合:
的盐酸等体积均匀混合:

D.在含有![]() 的溶液中加入
的溶液中加入![]() 再加入
再加入![]() ,则反应体系显紫红色:
,则反应体系显紫红色:

 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
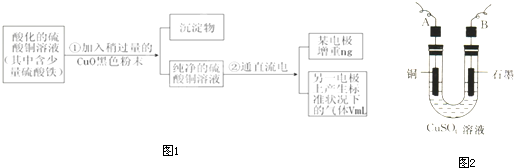
| ||
| ||
| 11200 |
| V |
| 11200 |
| V |
查看答案和解析>>
科目:高中化学 来源: 题型:
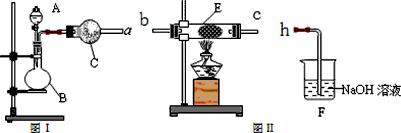
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
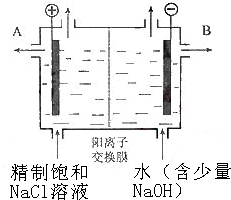 工业上电解制碱的技术是用离子交换膜法,主要原料是饱和食盐水.下图为离子交换膜法电解原理示意图:请回答下列问题:
工业上电解制碱的技术是用离子交换膜法,主要原料是饱和食盐水.下图为离子交换膜法电解原理示意图:请回答下列问题:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
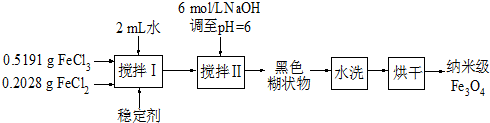
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ① | ② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com