
(10分)有以下物质:①Mg ②Al ③ C ④稀硫酸 ⑤浓硫酸 ⑥ NaOH溶液
(1)写出①与④反应的离子方程式 。
(2)既能跟④又能跟⑥反应的是 (填序号),写出它与⑥反应的化学方程式 。
(3)写出写出③与⑤反应的化学方程式 ,下列关于该反应中⑤体现的性质说法正确的是 。
a.既体现氧化性又体现酸性
b.只体现氧化性
c.只体现酸性
d.体现吸水性
(1)Mg+2H+ ══ Mg2++ H2↑
(2)② 2Al+ 2NaOH+ 2H2O══2 NaAlO2+3H2↑
C + 2H2SO4(浓) △ CO2↑+ 2SO2↑+ 2H2O(2分) b
【解析】
试题分析:(1)镁和稀硫酸反应生成硫酸镁和氢气,离子方程式为:Mg+2H+ ══ Mg2++ H2↑;(2)既能与稀硫酸反应,又能与氢氧化钠溶液反应的是铝(②),铝与氢氧化钠溶液反应的化学方程式为:2Al+ 2NaOH+ 2H2O══2 NaAlO2+3H2↑ ;(3)碳与浓硫酸反应产生二氧化碳、二氧化硫和水,反应方程式为:C + 2H2SO4(浓) △ CO2↑+ 2SO2↑+ 2H2O,在该反应中浓硫酸体现了强氧化性,故选b。
考点:考查元素及其化合物的性质。


科目:高中化学 来源:2014-2015湖南省浏阳市高二上学期理科化学试卷(解析版) 题型:选择题
在2A+B  3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A.v(A)= 0.5 mol/(L·s) B.v(B)= 0.3 mol/(L·s)
C.v(C)= 0.8 mol/(L·s) D.v(D)= 1 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省广州市高一上学期期末化学试卷(解析版) 题型:选择题
下列关于硅及化合物的用途正确的是
A.硅用于制光导纤维
B.二氧化硅用于制造太阳能电池
C.硅酸钠溶液是制木材防火剂的原料
D.“硅胶”是硅酸干凝胶,可用作催化剂的载体
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省广州市高一上学期期末化学试卷(解析版) 题型:选择题
下列物质,不能与CO2反应,但可以与SiO2反应的是
A.HF B.H2O C.CaO D.NaOH
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省广州市高一上学期期末化学试卷(解析版) 题型:选择题
下列行为符合安全要求的是
A.将水倒入浓硫酸中配制稀硫酸
B.金属钠着火,立即用泡沫灭火器灭火
C.炒菜时,油锅着火,应立即用锅盖盖灭
D.用点燃的火柴在液化气钢瓶口检验是否漏气
查看答案和解析>>
科目:高中化学 来源:2014-2015北京市昌平区高一上学期期末考试化学试卷(解析版) 题型:选择题
火法炼铜的原理为:Cu2S + O2 高温 2Cu + SO2,下列说法中,正确的是
A.Cu2S只作还原剂
B.该反应中的氧化剂只有O2
C.Cu2S 中的Cu元素被S元素还原
D.当1 mol O2参加反应时,共转移4 mol e-
查看答案和解析>>
科目:高中化学 来源:2014-2015北京市昌平区高一上学期期末考试化学试卷(解析版) 题型:选择题
对1 mol N2和1 mol CO2进行比较,下列说法不正确的是
A.分子数一定相同 B.原子数一定不相同
C.体积一定相同 D.质量一定不相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市黄浦区高三上学期期末调研测试化学试卷(解析版) 题型:计算题
(本题共14分)元素周期表中大多数元素是金属元素,金属及其化合物在生活生产中有着重要应用,根据试题信息,完成下列计算:
51.某常见二价金属12.6g与足量稀硫酸反应,生成氢气5.04L(S.T.P),该元素原子的摩尔质量为 g/mol。
52.39.32g某金属混合物,由12.32g镁和0.25mol另一种比镁不活泼的金属元素A组成,该混合物与一定量盐酸反应,产生氢气4.928L(S.T.P),则参加反应的HCl为 mol,金属A的相对原子质量为 。
53.由NaCl、NaHCO3、Na2CO3·10H2O组成的混合物157.8g,充分加热后,产生的气体(气体温度150℃)依次通过无水CaCl2和碱石灰,两种吸收剂分别增重59.4g和13.2g,则混合物中NaHCO3的质量分数为 ,若等质量的该混合物与足量盐酸反应,产生二氧化碳(S.T.P) L。
54.将一包铝热剂(铝粉和氧化铁的混合物)进行如下实验
①向一份铝热剂中加入800mL 2.0mol/L的NaOH溶液,使其充分反应后,收集到的气体体积为20.16L(S.T.P)。
②另一份等质量的铝热剂在高温下充分反应后,向反应后固体中加入2L 2.5mol/L的盐酸溶液,使固体完全溶解,反应后溶液pH=0(假设过程中溶液体积不变),取少量反应后溶液,滴加硫氰化钾,没有出现血红色。完成下列计算:
(1)计算该铝热剂中铝与氧化铁物质的量之比。
(2)实验②产生的气体体积是多少(S.T.P)?
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省资阳市高三第二次诊断性考试理综化学试卷(解析版) 题型:推断题
(15分)已知: 。
。

醇酸树脂是一种成膜性良好的树脂,下面是一种醇酸树脂的合成线路:
(1)B中含碳官能团的结构式为_____,C的名称是_____。
(2)反应①的有机反应类型是_____。
(3)下列说法正确的是_____(填字母编号)。
a.1 mol E与足量的银氨溶液反应能生成2 mol Ag
b.F能与NaHCO3反应产生CO2
c.检验CH3CH2CH2Br中的溴原子时,所加试剂的顺序依次是过量氢氧化钠溶液、硝酸银溶液
(4)写出E与新制的氢氧化铜悬浊液反应的化学方程式_____;
(5)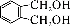 的同分异构体中同时符合下列条件的芳香族化合物共有_____种。
的同分异构体中同时符合下列条件的芳香族化合物共有_____种。
a.能发生消去反应 b.能与过量浓溴水反应生成白色沉淀
(6)写出反应⑤的化学方程式_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com