
”¾ĢāÄæ”æŗ£Ė®ŹĒ×ŌČ»ŁnøųČĖĄąµÄ±¦²Ų£¬ŗ£Ė®µÄ×ŪŗĻĄūÓĆŹĒČ«ŹĄ½ēŃŠ¾æµÄÖŲµć”£
Ķź³ÉĻĀĮŠĪŹĢā:
£Ø1£©“ÖŃĪÖŠ³żĮĖŗ¬ÓŠÄąÉ³Ö®Ķā»¹ŗ¬ÓŠCa2+”¢Mg2+”¢SO42-µČŌÓÖŹ£¬“ÖŃĪ»ńµĆ¾«ŃĪŅ»°ć²½Öč:

¼ÓČėĀČ»Æ±µ”¢“æ¼īŗĶÉÕ¼īµÄÄæµÄŅĄ“ĪŹĒ:_________”¢_________”¢_________”£
£Ø2£©ŗ£Ė®ĢįČ”½šŹōĆ¾Į÷³ĢČēĻĀ:

Į÷³ĢÖŠ¼ÓČėŹģŹÆ»ŅÄæµÄ__________£»³ĮµķÓėŃĪĖį·“Ó¦µÄĄė×Ó·½³ĢŹ½_____________”£
£Ø3£©Ä³Ń§ÉśŹµŃéŹŅÄ£ÄāŗÓĖ®ĢįČ”äåµÄ²½ÖčĪŖ:ŗ£Ė®”śÅØĖõ”śŃõ»Æ”śĢįČ””śäå
¢ŁŃõ»Æ²½Öč:ŹŹŠū×÷Ńõ»Æ¼ĮµÄŹĒ_______”£
ABr2 B.Cl2 C.I2 DHCl
¢ŚĢįČ”²½Öč£ŗ””äåĖ®ÖŠ¼ÓČėCCl4Õńµ“”¢¾²ÖĆ””µĆäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗ£¬øĆ·ÖĄėĢį“æäåµÄ·½·Ø½Š________£»ÓƵ½µÄÖ÷ŅŖŅĒĘ÷ĪŖ________”£
£Ø4£©ŹµŃéÖ¤Ć÷½šŹōÖĘĘ·ŌŚŗ£Ė®ÖŠøüČŻŅ×ÉśŠā£¬ĶŠāµÄ»ÆѧŹ½ĪŖ: ________£»CuÓėĮņ»Ē·“Ó¦µÄ»Æѧ·½³ĢŹ½________£»
”¾“š°ø”æ ³żSO42- ³żCa2+ŗĶBa2+ ³żMg2+ Ź¹Mg2+³Įµķ Mg(OH)2+2H+=2H2O +Mg2+ B .ŻĶČ”·ÖŅŗ£Ø»ņŻĶČ”£© ·ÖŅŗĀ©¶· Cu2(OH)2CO3 2Cu+S![]() Cu2S
Cu2S
”¾½āĪö”æ£Ø1£©¼ÓČėĀČ»Æ±µČÜŅŗ”£³żČ„ČÜŅŗÖŠµÄSO42-£»¼ÓČė“æ¼īČÜŅŗ³żČ„ČÜŅŗÖŠCa2+ŗĶBa2+£»¼ÓČėÉÕ¼īČÜŅŗ³żČ„ČÜŅŗÖŠµÄMg2+”£ÕżČ·“š°ø£ŗ³żSO42- £»³żCa2+ŗĶBa2+£» ³żMg2+”£
£Ø2£©°Ńŗ£Ė®ÖŠĆ¾Ąė×Ó±äĪŖĒāŃõ»ÆĆ¾³Įµķ£¬±ćÓŚø»¼ÆĆ¾ŌŖĖŲ£»ĒāŃõ»ÆĆ¾ÓėŃĪĖį·“Ӧɜ³ÉĀČ»ÆĆ¾ČÜŅŗŗĶĖ®£»ÕżČ·“š°ø£ŗŹ¹Mg2+³Įµķ£»Mg(OH)2+2H+=2H2O +Mg2+ ”£
£Ø3£©¢ŁŃõ»ÆŠŌ£ŗ.Cl2>Br2>I2 > HCl£¬ŹŹŅĖµÄŃõ»Æ¼ĮĪŖCl2£¬ĀČĘųÄܹ»°ŃäåĄė×ÓŃõ»ÆĪŖäåµ„ÖŹ£»ÕżČ·Ń”Ļī£ŗB”£
¢Ś ÓĆĖÄĀČ»ÆĢ¼°Ńäå“ÓäåĖ®ČÜŅŗÖŠŻĶČ”³öĄ“£¬äå½ųČėĖÄĀČ»ÆĢ¼ÖŠ£¬ŗĶĖ®·Ö²ć£¬½ųŠŠ·ÖŅŗ£¬ÓƵ½µÄŅĒĘ÷ĪŖ·ÖŅŗĀ©¶·£»ÕżČ·“š°ø£ŗŻĶČ”·ÖŅŗ£Ø»ņŻĶČ”£©£» ·ÖŅŗĀ©¶·”£
£Ø4£©½šŹōĶÓėŃõĘų”¢¶žŃõ»ÆĢ¼”¢Ė®µČ»ģŗĻ·“Ӧɜ³É¼īŹ½Ģ¼ĖįĶ£»ÕżČ·“š°ø£ŗCu2(OH)2CO3”£ĮņµÄŃõ»ÆŠŌČõ£¬Ö»ÄÜ°ŃĶŃõ»ÆĪŖ+1¼Ū£¬½šŹōĶÓėĮņ¼ÓČČ·“Ӧɜ³ÉĮņ»ÆŃĒĶ£»ÕżČ·“š°ø£ŗ2Cu+S![]() Cu2S”£
Cu2Sӣ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijČÜŅŗÖŠŗ¬ÓŠHCO3©”¢SO32©”¢Cl©ŗĶNa+ £¬ ČōĻņĘäÖŠĶØČė×ćĮæµÄCl2 £¬ ČÜŅŗÖŠÉĻŹöĖÄÖÖĄė×ÓµÄÅØ¶Č»ł±¾±£³Ö²»±äµÄŹĒ£Ø £©
A.HCO3©
B.SO32©
C.Cl©
D.Na+
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA~JŹĒ³£¼ūµÄ»ÆѧĪļÖŹ£¬×Ŗ»Æ¹ŲĻµČēĻĀĶ¼ĖłŹ¾”£AŹĒÉś»īÖŠµÄŅ»ÖÖµ÷Ī¶¼Į£¬IŹĒŅ»ÖÖÓĆĶ¾¹ć·ŗµÄ½šŹō£¬³£ĪĀĻĀC”¢D”¢E”¢F”¢J½ŌĪŖĘųĢ壬 HÓÉĮ½ÖÖŌŖĖŲ¹¹³É£¬Ä¦¶ūÖŹĮæĪŖ41 g”¤mol£1”£

£Ø1£©IµÄ»ÆѧŹ½ĪŖ________,HµÄ»ÆѧŹ½ĪŖ________”£
£Ø2£©Š“³ö·“Ó¦¢Ł¢Ś¢Ū¢ÜµÄ»Æѧ·½³ĢŹ½
¢Ł_______£»¢Ś________£» ¢Ū_______£» ¢Ü________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķŹĒŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö£¬Õė¶Ō±ķÖŠµÄ¢Ł”«¢ąÖÖŌŖĖŲ£¬ĢīŠ“ĻĀĮŠæÕ°×£ŗ
Ö÷×å ÖÜĘŚ | ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A |
2 | ¢Ł | ¢Ś | ¢Ū | ¢Ü | |||
3 | ¢Ż | ¢Ž | ¢ß | ¢ą |
£Ø1£©ŌŚ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļÖŠ£¬ĖįŠŌ×īĒæµÄ»ÆŗĻĪļµÄĆū³ĘŹĒ______£¬¼īŠŌ×īĒæµÄ»ÆŗĻĪļµÄ»ÆѧŹ½ŹĒ_______”£
£Ø2£©¢Ż¢ßŠĪ³É»ÆŗĻĪļµÄµē×ÓŹ½___”£¢ŚŠĪ³ÉµÄ×īøß¼ŪŃõ»ÆĪļµÄ½į¹¹Ź½____”£
£Ø3£©×īøß¼ŪŃõ»ÆĪļŹĒĮ½ŠŌŃõ»ÆĪļµÄŌŖĖŲĘäŌŖĖŲ·ūŗÅŹĒ____£»Š“³öĖüµÄĒāŃõ»ÆĪļÓė¢ąµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ·“Ó¦µÄĄė×Ó·½³ĢŹ½________”£
£Ø4£©¢ŽµÄµ„ÖŹÓė¢ŻµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ______”£
£Ø5£©¢ŚŗĶ¢ßæÉŠĪ³ÉŌ×ÓŹż1”Ć2µÄŅŗĢ¬»ÆŗĻĪļ¼×£¬²¢ÄÜČܽā¢ßµÄµ„ÖŹ£¬ÓƵē×ÓŹ½±ķŹ¾¼×µÄŠĪ³É¹ż³Ģ£ŗ____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĶ¬Ń§ŌŚ×öÅØĮņĖįÓėĶ·“Ó¦µÄŹµŃé¹ż³ĢÖŠ£¬¹Ū²ģµ½Ķʬ±ķĆę±äŗŚ£¬ÓŚŹĒ¶ŌŗŚÉ«ĪļÖŹµÄ×é³É½ųŠŠŹµŃéĢ½¾æ”£
£Ø1£©ÓĆČēÓŅĶ¼ĖłŹ¾×°ÖĆ½ųŠŠŹµŃé1”££Ø¼ÓČČŗĶ¼Š³ÖŅĒĘ÷ŅŃĀŌČ„£©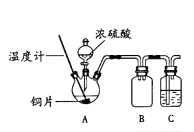
ŹµŃé1£ŗĶʬÓėÅØĮņĖį·“Ó¦
²Ł×÷ | ĻÖĻó |
¼ÓČȵ½120”ę~250”ę | Ķʬ±ķĆę±äŗŚ£¬ÓŠ“óĮæĘųĢå²śÉś£¬ŠĪ³ÉÄ«ĀĢÉ«×ĒŅŗ |
¼ĢŠų¼ÓČČÖĮ338”ę | ĶʬÉĻŗŚÉ«ĻūŹ§£¬ĘæÖŠ³öĻÖ”°°×Īķ”±£¬ČÜŅŗĀŌ“ųĄ¶É«£¬Ęæµ×²æÓŠ½Ļ¶ą»Ņ°×É«³Įµķ |
¢Ł×°ÖĆBµÄ×÷ÓĆŹĒ£»×°ÖĆCÖŠŹ¢·ÅµÄŹŌ¼ĮŹĒ”£
¢ŚĪŖÖ¤Ć÷A×°ÖĆÖŠ»Ņ°×É«³ĮµķµÄÖ÷ŅŖ³É·ÖĪŖĮņĖįĶ£¬ŹµŃé²Ł×÷¼°ĻÖĻóŹĒ”£
£Ø2£©Ģ½¾æŹµŃé1ÖŠ120”ę~250”ꏱĖłµĆŗŚÉ«¹ĢĢåµÄ³É·Ö”£
”¾Ģį³ö²ĀĻė”æŗŚÉ«¹ĢĢåÖŠæÉÄÜŗ¬ÓŠCuO”¢CuS”¢Cu2SÖŠµÄŅ»ÖÖ»ņ¼øÖÖ”£
”¾²éŌÄ׏ĮĻ”æ
׏ĮĻ1£ŗŃĒĢśĒč»Æ¼Ų[K4Fe(CN£©6]ŹĒCu2+µÄĮéĆō¼ģ²ā¼Į£¬Ļņŗ¬ÓŠCu2+µÄČÜŅŗÖŠµĪ¼ÓŃĒĢśĒč»Æ¼ŲČÜŅŗ£¬Éś³Éŗģ×ŲÉ«³Įµķ”£
׏ĮĻ2£ŗ
CuS | Cu2S |
ŗŚÉ«½į¾§»ņ·ŪÄ© | »ŅŗŚÉ«½į¾§»ņ·ŪÄ© |
ÄŃČÜÓŚĻ”ĮņĖį£»æÉČÜÓŚĻõĖį£»Ī¢ČÜÓŚÅØ°±Ė®»ņČȵÄÅØŃĪĖį | ÄŃČÜÓŚĻ”ĮņĖįŗĶÅØŃĪĖį£»æÉČÜÓŚĻõĖį£»Ī¢ČÜÓŚÅØ°±Ė® |
”¾Éč¼Ę²¢ŹµŹ©ŹµŃé”æ
ŹµŃé2.Ģ½¾æŗŚÉ«¹ĢĢåÖŠŹĒ·ńŗ¬CuO
²Ł×÷ | ĻÖĻó |
i.Č”±ķĆęø½×ÅŗŚÉ«¹ĢĢåµÄĶʬ5ʬ£¬ÓĆĒåĖ®Ļ“øɾ»£¬·ÅČėŹ¢ÓŠ10mLŹŌ¼ĮAµÄŠ”ÉÕ±ÖŠ£¬½Į°č | ŗŚÉ«±ķ²ćĶŃĀ䣬Ā¶³ö¹āĮĮµÄĶʬ |
ii.Č”³öĶʬ£¬“żŗŚÉ«³Įµķ³Į½µ | ÉĻ²ćČÜŅŗ³ĪĒ唢ĪŽÉ« |
¢ŁŹŌ¼ĮAŹĒ”£
¢Ś¼×ČĻĪŖiiÖŠČÜŅŗĪŽÉ«ÓŠæÉÄÜŹĒCu2+ÅضČĢ«Š”£¬ÓŚŹĒ²¹³äŹµŃéČ·ČĻĮĖČÜŅŗÖŠ²»ŗ¬Cu2+ £¬ ²¹³äµÄŹµŃé²Ł×÷¼°ĻÖĻóŹĒ”£
ŹµŃé3.Ģ½¾æŗŚÉ«¹ĢĢåÖŠŹĒ·ńŗ¬CuS”¢Cu2S
²Ł×÷ | ĻÖĻó |
i.Č”ŹµŃé2ÖŠŗŚÉ«¹ĢĢåÉŁŠķ£¬¼ÓČėŹŹĮæÅØ°±Ė®£¬Õńµ“ŗó¾²ÖĆ | ÓŠ¹ĢĢåŹ£Óą£¬¹ĢŅŗ·Ö½ēĻßø½½üµÄČÜŅŗ³ŹĒ³Ą¶É« |
ii.ĮķČ”ŹµŃé2ÖŠŗŚÉ«¹ĢĢåÉŁŠķ£¬¼ÓČėŹŹĮæÅØŃĪĖį£¬Ī¢ČČŗó¾²ÖĆ | ÓŠ¹ĢĢåŹ£Óą£¬ČÜŅŗ±ä³ÉĒ³ĀĢÉ« |
”¾»ńµĆ½įĀŪ”æÓÉŹµŃé2ŗĶŹµŃé3æɵƵ½µÄ½įĀŪŹĒ£ŗŹµŃé1ÖŠ£¬120”ę~250”ꏱĖłµĆŗŚÉ«¹ĢĢåÖŠ”£
”¾ŹµŃé·“Ė¼”æ
·ÖĪöŹµŃé1ÖŠ338”ꏱ²śÉśĻÖĻóµÄŌŅņ£¬Ķ¬Ń§ĆĒČĻĪŖŹĒ½ĻµĶĪĀ¶ČŹ±²śÉśµÄŗŚÉ«¹ĢĢåÓėČȵÄÅØĮņĖį½ųŅ»²½·“Ó¦Ōģ³É”£ŅŃÖŖ·“Ó¦µÄŗ¬Įņ²śĪļ³żĪŽĖ®ĮņĖįĶĶā»¹ÓŠ¶žŃõ»ÆĮņ£¬ŌņŗŚÉ«¹ĢĢåĻūŹ§Ź±æÉÄÜ·¢ÉśµÄĖłÓŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖ¼ÓĖŁĘÆ·Ū¾«µÄĻū¶¾×÷ÓĆ£¬×īŗƵķ½·ØŹĒ
A.ÓĆĖ®ČܽāB.¼ÓČėÉŁĮæĻ”ŃĪĖįC.øÉŌļŗóŹ¹ÓĆD.¼ÓČėNaOHČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ·“Ó¦Ņ»¶ØŹōÓŚŃõ»Æ»¹Ō·“Ó¦µÄŹĒ£Ø £©
A.»ÆŗĻ·“Ó¦
B.ÖĆ»»·“Ó¦
C.·Ö½ā·“Ó¦
D.ø“·Ö½ā·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬Ļņ100mL0.01mol/LµÄHAČÜŅŗÖŠÖšµĪ¼ÓČė0.02mol/LµÄMOHČÜŅŗ£¬Ķ¼ÖŠĖłŹ¾ĒśĻß±ķŹ¾»ģŗĻČÜŅŗµÄpHµÄ±ä»ÆĒéæö£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £© 
A.ŌŚNµ½K¼äČĪŅāŅ»µć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗc£ØM+£©+c£ØH+£©=c£ØOH”„£©+c£ØA”„£©
B.HAĪŖČõĖį
C.³£ĪĀĻĀ£¬MAČÜŅŗµÄpH£¾7
D.NµćĖ®µÄµēĄė³Ģ¶ČŠ”ÓŚKµćĖ®µÄµēĄė³Ģ¶Č
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»ŗćČŻµÄĆܱÕČŻĘ÷ÖŠ³äČė 0.1mol/L CO2”¢0.1mol/L CH4 £¬ ŌŚŅ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗCH4£Øg£©+CO2£Øg£©2CO£Øg£©+2H2£Øg£©£¬²āµĆCH4Ę½ŗāŹ±×Ŗ»ÆĀŹÓėĪĀ¶Č”¢Ń¹Ēæ¹ŲĻµČēĶ¼£¬ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £© 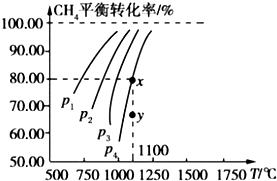
A.1100”ꏱøĆ·“Ó¦Ę½ŗā³£ŹżĪŖ 1.64
B.Ń¹Ēæ£ŗp4£¾p3£¾p2£¾p1
C.ÉĻŹö·“Ó¦µÄ”÷H£¼0
D.Ń¹ĒæĪŖ p4Ź±£¬ŌŚyµć£ŗv Õż£¾v Äę
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com