
【题目】A~H8种物质存在如下转化关系(反应条件,部分产物未标出)。已知:A是酸式盐,B是能使品红溶液褪色的气体,G是红棕色气体。按要求回答问题:
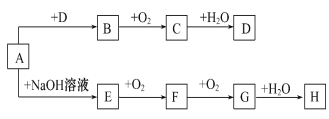
(1)写出下列物质的化学式:A___________。
(2)写出下列反应的化学方程式:
B与E按1:2通入水中_________;
G→H_______
D的浓溶液与红热的木炭反应的方程式:______
(3)检验某溶液中是否含D中阴离子的方法:__________________。
【答案】NH4HSO3 2NH3+SO2+H2O =(NH4)2SO3 3NO2+H2O====2HNO3+NO C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O 取少量被检验溶液注入一支试管中,然后向试管中滴加盐酸,溶液无明显现象,然后滴加BaCl2溶液,若产生白色沉淀,说明溶液中存在SO42-,否则溶液中不存在SO42-
CO2↑+2SO2↑+2H2O 取少量被检验溶液注入一支试管中,然后向试管中滴加盐酸,溶液无明显现象,然后滴加BaCl2溶液,若产生白色沉淀,说明溶液中存在SO42-,否则溶液中不存在SO42-
【解析】
G是红棕色气体,则G是NO2,F和氧气反应生成二氧化氮,所以F是NO,二氧化氮和水反应生成H是HNO3.A是酸式盐,和氢氧化钠反应生成E,E和氧气反应生成NO,则E是NH3,B能使品红溶液褪色,且B能和氧气反应生成C,所以B是SO2,C是SO3,三氧化硫和水反应生成D为H2SO4,A是酸式盐且是铵盐,所以A是NH4HSO3,据此答题。
由分析可知:A是NH4HSO3,B是SO2,C是SO3,D为H2SO4,E是NH3,F是NO,G是NO2,H是HNO3。
(1)通过以上分析可知,A是NH4HSO3,故答案为:NH4HSO3。
(2)SO2与NH3按1:2通入水中反应生成亚硫酸铵,反应方程式为2NH3+SO2+H2O=(NH4)2SO3;G→H为二氧化氮与水反应生成硝酸与一氧化氮,反应方程式为3NO2+H2O=2HNO3+NO;木炭和浓硫酸在加热条件下反应生成二氧化硫、二氧化碳和水,反应方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;故答案为:2NH3+SO2+H2O=(NH4)2SO3;3NO2+H2O=2HNO3+NO;C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O;故答案为:2NH3+SO2+H2O=(NH4)2SO3;3NO2+H2O=2HNO3+NO;C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(3)D为H2SO4,其阴离子为SO42-,SO42-的检验方法为:取少量被检验溶液注入一支试管中,然后向试管中滴加盐酸,溶液无明显现象,然后滴加BaCl2溶液,若产生白色沉淀,说明溶液中存在SO42-,否则溶液中不存在SO42-,故答案为:取少量被检验溶液注入一支试管中,然后向试管中滴加盐酸,溶液无明显现象,然后滴加BaCl2溶液,若产生白色沉淀,说明溶液中存在SO42-,否则溶液中不存在SO42-。


科目:高中化学 来源: 题型:
【题目】根据下列事实得出的结论正确的是
A. 试样![]() 产生银镜 结论:该试样是醛类
产生银镜 结论:该试样是醛类
B. 某卤代烃试样![]() 最终的沉淀不是白色;结论:该卤代烃中不含氯原子
最终的沉淀不是白色;结论:该卤代烃中不含氯原子
C. 往淀粉溶液中加入稀硫酸并且加热一段时间,再加入新制的氢氧化铜悬蚀液再加热。发现没有红色沉淀生成;结论: 淀粉没有水解生成葡萄糖
D. 将溴乙烷和NaOH的醇溶液混合加热,得到的气体先通入水中再通入酸性KMnO4溶液,溶溶褪色,说明发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将适量铁粉放入三氯化铁溶液中,完全反应后,溶液中c(Fe3+)=2c(Fe2+)。则已反应的Fe3+和未反应的Fe3+的物质的量之比是( )
A. 2:3B. 3:2C. 1:3D. 1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B两种烃,其相关信息如下:
A ①完全燃烧的产物中n(CO2):n(H2O)=2:1
②28<M (A)<60
③不能使溴的四氯化碳溶液褪色④一氯代物只有一种结构
B ①饱和链烃,通常情况下呈气态②有同分异构体
③二溴代物有三种
回答下列问题:
(1)烃A的实验式是 ;
(2)烃A的结构简式是 ;
(3)烃B的三种二溴代物的结构简式为 、 、 ;
(4)烃C为烃B的同系物,常温下为气态且只有一种一溴代物,则烃C的一溴代物的结构简式为 (填一种即可).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
上述元素可组成盐R:zx4f(gd4)2。向盛有10mL 1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:

(1)R溶液中,离子浓度由大到小的顺序是___________________________________
(2)写出m点反应的离子方程式:__________________________________________。
(3)若在R溶液中改加20mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验来探究元素周期律。
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;

(1)写出选用物质的名称:A_________,B________,C________;上述反应的离子方程式____________;___________。
乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。
已知常温下浓盐酸与高锰酸钾能反应生成氯气。
(2)乙同学的实验原理是 _______________,写出B处的离子方程式: _______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com