
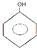
 六种物质中:
六种物质中:分析 ①能与溴水发生化学反应的物质可含有不饱和键或含为酚类物质;
②属于高分子化合物的多为高聚物;
③能与Na2CO3溶液反应的是物质可为酸;
④能发生酯化反应的物质含有羟基或羧基;
⑤能发生消去反应的为醇或卤代烃.
解答 解:①能与溴水发生化学反应的物质可含有不饱和键或含为酚类物质,则①⑥符合,故答案为:①⑥;
②属于高分子化合物的多为高聚物,则⑤符合,故答案为:⑤;
③能与Na2CO3溶液反应的是物质可为酸,则④⑥符合,故答案为:④⑥;
④能发生酯化反应的物质含有羟基或羧基,则③④符合,故答案为:③④;
⑤能发生消去反应的为醇或卤代烃,则②③符合,故答案为:②③.
点评 本题考查了有机物结构与性质、有机反应类型判断,题目难度中等,注意掌握常见有机物的结构与性质,明确常见的烃的衍生物官能团与反应类型之间的关系.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
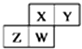 如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )| A. | 原子半径:W>Z>Y>X | |
| B. | 气态氢化物的稳定性:Z>W>X>Y | |
| C. | W的最高正化合价与负化合价的绝对值可能相等 | |
| D. | Z的最高价氧化物的水化物一定为强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 牙膏品牌 | 青蛙儿童牙膏 | 佳洁士盐白牙膏 | 中华透明牙膏 |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
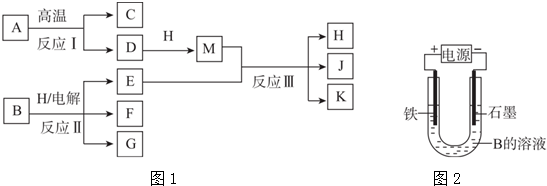
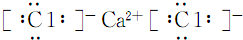 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
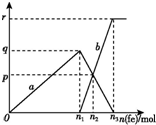 含有1 mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示.下列有关判断正确的是( )
含有1 mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示.下列有关判断正确的是( )| A. | a是Fe(NO3)2 | B. | n1=0.375 | C. | p=0.125 | D. | n2=0.30 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com