
【题目】下列分子的稳定性的比较正确的是( )
A. HF>HI B. CH4<SiH4 C. PH3>NH3 D. H2O<H2S
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:
【题目】硅是重要的半导体材料,构成了现代电子工业的基础。回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号为__,该能层所含的能级数为__,电子数为__。
(2)在SiO44-中Si原子的杂化形式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通入Cl2过程中溶液内发生反应的离子方程式,其中不正确的是( )
A. x=0.4a,2Fe2++Cl2===2Fe3++2Cl-
B. x=0.6a,2Br-+Cl2===Br2+2Cl-
C. x=a,2Fe2++2Br-+2Cl2===Br2+2Fe3++4Cl-
D. x=1.5a,2Fe2++4Br-+3Cl2===2Br2+2Fe3++6Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于离子键、共价键的各种叙述中,下列说法中正确的是
A.在离子化合物里,只存在离子键,没有共价键
B.非极性键只存在于双原子的单质分子(如Cl2)中
C.在共价化合物分子内,一定不存在离子键
D.由不同元素组成的多原子分子里,一定只存在极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含a mol NaOH和a mol Na2CO3的混合溶液中通入b mol CO2充分反应(不考虑CO2的溶解),下列说法不正确的是( )
A. 当a≥2b时,发生的离子反应为2OH-+CO2===CO![]() +H2O
+H2O
B. 当a=1.25b时,发生的离子方程式为5OH-+4CO2===3HCO![]() +CO
+CO![]() +H2O
+H2O
C. ![]() <a<2b时,溶液中CO
<a<2b时,溶液中CO![]() 与HCO
与HCO![]() 物质的量之比为(2b-a)∶(2a-b)
物质的量之比为(2b-a)∶(2a-b)
D. 若反应后溶液中CO![]() 与OH-物质的量之比为2∶1,则5b=a
与OH-物质的量之比为2∶1,则5b=a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
A. 标准状况时,22.4L二氯甲烷所含有的分子数为NA
B. 将16gO2与32gSO2在一定的条件下充分反应生成的SO3分子数为0.5NA
C. lmolNa2O2中含有的阴、阳离子总数是4NA
D. 44g丙烷中含有的非极性键数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知还原性:SO![]() >I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )
>I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )
A. 当a≥b时,发生的离子反应为SO![]() +Cl2+H2O===SO
+Cl2+H2O===SO![]() +2H++2Cl-
+2H++2Cl-
B. 当5a=4b时,发生的离子反应为4SO![]() +2I-+5Cl2+4H2O===4SO
+2I-+5Cl2+4H2O===4SO![]() +I2+8H++10Cl-
+I2+8H++10Cl-
C. 当a≤b≤![]() a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol
a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol
D. 当a<b<![]() a时,溶液中SO
a时,溶液中SO![]() 、I-与Cl-的物质的量之比为a∶(3a-2b)∶2b
、I-与Cl-的物质的量之比为a∶(3a-2b)∶2b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是关于有机物A、B的信息:
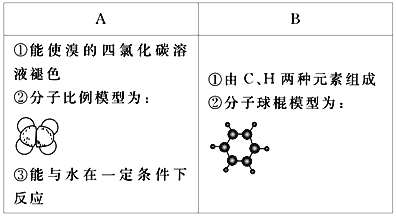
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称为________;写出在一定条件下,A发生聚合反应生成高分子化合物的方程式___________________________________________。
(2)A的同系物用通式CnHm表示,B的同系物用通式CxHy表示,当CnHm、CxHy分别出现属于同类物质的同分异构体(分别为A、B的同系物)时,碳原子数的最小值n=______,x=________。
(3)B具有的性质是________。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤能使酸性KMnO4溶液和溴水褪色 ⑥任何条件下均不与氢气反应 ⑦与溴水混合后液体分层且上层呈橙红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是()
A.需要加热才能进行的反应是吸热反应
B.CH3COOH+KOH=CH3COOK+H2O这个反应为吸热反应
C.反应放出热量的多少与反应物的质量和状态无关
D.若氢气和氧气化合是放热反应,则水电解生成氢气和氧气是吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com