
分析 C可用做果实催熟剂,则C为CH2=CH2,C可由B与浓硫酸混合加热制得,则B为CH3CH2OH,一溴代烷A与氢氧化钠溶液混合后充分振荡,生成有机物,则A为CH3CH2Br,再结合问题分析解答.
解答 解:C可用做果实催熟剂,则C为CH2=CH2,C可由B与浓硫酸混合加热制得,则B为CH3CH2OH,一溴代烷A与氢氧化钠溶液混合后充分振荡,生成有机物,则A为CH3CH2Br,
(1)A是溴乙烷,结构简式为CH3CH2Br,故答案为:CH3CH2Br;
(2)A是溴乙烷、B是乙醇,溴乙烷和NaOH的水溶液发生水解反应生成乙醇,A生成B的化学方程式为CH3CH2Br+NaOH$\stackrel{H_{2}O}{→}$CH3CH2OH+NaBr,故答案为:CH3CH2Br+NaOH$\stackrel{H_{2}O}{→}$CH3CH2OH+NaBr;
(3)A是溴乙烷、C是乙烯,溴乙烷和NaOH的醇溶液加热生成乙烯,反应方程式为CH3CH2Br+NaOH$→_{△}^{乙醇}$CH2=CH2↑+NaBr+H2O,
故答案为:CH3CH2Br+NaOH$→_{△}^{乙醇}$CH2=CH2↑+NaBr+H2O;
(4)B发生消去反应生成C,反应类型是消去反应,故答案为:消去反应.
点评 本题考查有机物推断,为高频考点,涉及卤代烃、醇、烯烃之间的转化,明确官能团及其性质关系、常见有机反应类型是解本题关键,注意卤代烃发生消去反应和水解反应区别,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 )是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下:
)是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下:


 .
. .
. .
. .
. 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2Br$→_{加热}^{NaOH/醇}$CH2=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH.
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2Br$→_{加热}^{NaOH/醇}$CH2=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强电解质一定是离子化合物,弱电解质一定是共价化合物 | |
| B. | 强电解质一定是易溶化合物,弱电解质一定是难溶化合物 | |
| C. | SO3溶于水后水溶液导电性很强,所以SO3是强电解质 | |
| D. | 强电解质与弱电解质的本质区别是在水溶液中能否完全电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
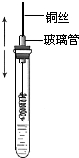 某同学在学习乙醇的知识后,设计了如下的实验. 操作步骤为:
某同学在学习乙醇的知识后,设计了如下的实验. 操作步骤为:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
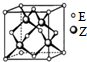 X、Y、Z、R、W、E为前四周期元素且原子序数依次增大.X的单质与Y的单质在放电条件下反应产生大气污染物,R基态原子的M能层上有3对成对电子,W核外有5个未成对电子.Y、Z分别形成氢化物Q和J,已知Q与J摩尔质量相等,Q的水溶液中加入少量WY2,立即产生大量气泡.E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:
X、Y、Z、R、W、E为前四周期元素且原子序数依次增大.X的单质与Y的单质在放电条件下反应产生大气污染物,R基态原子的M能层上有3对成对电子,W核外有5个未成对电子.Y、Z分别形成氢化物Q和J,已知Q与J摩尔质量相等,Q的水溶液中加入少量WY2,立即产生大量气泡.E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定含有I-,不能确定是否含有Cl- | B. | 一定含有NO3- | ||
| C. | 不含有Fe3+,可能含有NO3- | D. | 一定含有I-、NO3-和Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)某有机物含碳85.7%、氢14.3%,向80g含溴5%的溴水中通入该有机物,溴水恰好完全褪色,此时液体总重81.4g.
(1)某有机物含碳85.7%、氢14.3%,向80g含溴5%的溴水中通入该有机物,溴水恰好完全褪色,此时液体总重81.4g. .任选其中一种写出其生成高聚物的化学方程式
.任选其中一种写出其生成高聚物的化学方程式 (或
(或
 +3HNO3
+3HNO3
 +3H2O.
+3H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
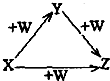
| A. | ①②③ | B. | ①② | C. | ③④ | D. | ①③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com