
分析 NO2和NO的混合气体通入倒立于水槽中盛满水的试管中,发生反应为3NO2+H2O=2HNO3+NO,导致气体体积减小,根据气体体积减少利用差量法计算二氧化氮气体的体积,再根据混合气体的体积计算一氧化氮气体的体积.
解答 解:设二氧化氮气体的体积为V,则:
3NO2+H2O=2HNO3+NO△V(气体体积减少)
3 2 1 2
V(NO2) 15mL-8mL=7mL
3:2=V(NO2):7mL,
V(NO2)=10.5mL,
原气体中V(NO)=15ml-10.5mL=4.5mL,
答:原混合气体中含有10.5mL二氧化氮、4.5mLNO.
点评 本题考查了根据方程式的计算,题目难度中等,关键是理解气体体积减少的原因,再利用差量法来分析解答,试题培养了学生的分析能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 它可作耐磨材料 | |
| B. | 它不可用作致冷剂 | |
| C. | 晶体中每个碳原子形成2个碳氧双键 | |
| D. | 晶体中碳、氧原子个数之比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
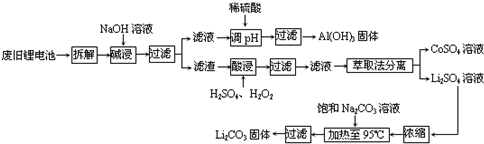
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
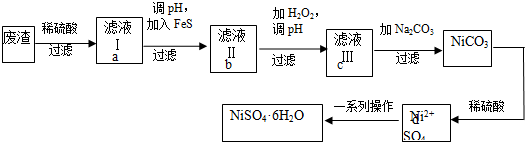
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com