
| A、0.5mol |
| B、0.8mol |
| C、1.1mol |
| D、1.2mol |
| 11.2L |
| 22.4L/mol |
| 19.2g |
| 64g/mol |


科目:高中化学 来源: 题型:
| A、从海水中可得到NaCl,电解熔融NaCl或其水溶液都可制得Cl2 |
| B、因海水中含有镁元素,故不需经过化学变化就可以得到镁单质 |
| C、利用蒸馏原理从海水中提取淡水是海水淡化技术发展的新方向 |
| D、无论是海水波浪发电还是潮汐发电,都是将化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化氮 | B、二氧化碳 |
| C、二氧化硫 | D、一氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA |
| B、78 g苯含有C=C双键的数目为3 NA |
| C、1 L 1 mol?L-1的NaClO溶液中含有ClO-的数目为NA |
| D、标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 化合价 | -4 | -1 | +1 | -4 | -2 |
| A、丙的常见氧化物有两种 |
| B、气态氢化物稳定性:丁>戊 |
| C、丁的氧化物能与乙的氢化物的水溶液反应 |
| D、原子半径大小:丙<丁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
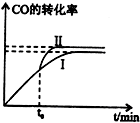 二甲醚是一种重要的清洁燃料,有多种合成方法.
二甲醚是一种重要的清洁燃料,有多种合成方法.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com