
【题目】关于化学反应的本质的说法正确的是( )
A.化学反应都有新物质生成
B.化学反应都有能量变化
C.化学反应是旧键断裂新键形成的过程
D.化学反应的发生都需要在一定条件下
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】如图是产生和收集气体的实验装置,该装置最适合于( )
A.用浓硝酸和Cu反应制取NO2
B.用浓盐酸和MnO2反应制取Cl2
C.用NH4Cl和Ca(OH)2反应制取NH3
D.用H2O2溶液和MnO2反应制取O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的的是( )
A.用图1所示装置除去Cl2中含有的少量HCl
B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图3所示装置制取少量纯净的CO2气体
D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某晶体(结晶水合物)由五种短周期元素组成.常温下,将该晶体溶于蒸馏水后可电离出三种离子(忽略水的电离),其中两种离子含有的电子数均为10个.将该溶液分成等量2份,一份中加入足量稀盐酸,无明显现象,再加入BaCl2溶液,产生白色沉淀;向另一份中逐滴加入NaOH溶液至过量,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示. 
请回答下列问题:
(1)若该晶体的摩尔质量为906gmol﹣1 , 写出该晶体的化学式;
(2)B点溶液的pH7(填“<”、“>”或“=”),用化学用语表示其原因 .
(3)若向该晶体的水溶液中逐滴加入Ba(OH)2溶液至产生最多的沉淀,写出该变化的离子方程式 .
(4)C点溶液中所含溶质的化学式为;此时溶液中各种离子浓度由大到小顺序为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了一个有一个奇迹.
(1)新型陶瓷Si3N4的熔点高、硬度大、化学性质稳定.工业上可以采用化学气相沉积法,在H2的保护下,使SiCl4与N2反应生成Si3N4沉积在石墨表面,写出该反应的化学方程式 .
(2)一种用工业硅(含少量钾、钠、铁、铜的氧化物),已知硅的熔点是1420℃,高温下氧气及水蒸气能明显腐蚀氮化硅.一种合成氮化硅的工艺主要流程如图: 
①净化N2和H2时,铜屑的作用是:;硅胶的作用是 .
②在氮化炉中3SiO2(s)+2N2(g)═Si3N4(s)△H=﹣727.5kJ/mol,开始时为什么要严格控制氮气的流速以控制温度;体系中要通入适量的氢气是为了 .
③X可能是(选填:“盐酸”、“硝酸”、“硫酸”、“氢氟酸”).
(3)工业上可以通过如图所示的流程制取纯硅:
①整个制备过程必须严格控制无水无氧.SiHCl3遇水剧烈反应,写出该反应的化学方程式 .
②假设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应Ⅰ中HCl的利用率为90%,反应Ⅱ中H2的利用率为93.75%.则在第二轮次的生产中,补充投入HCl和H2的物质的量之比是 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和CO是合成许多有机物的原料,有如下反应:mH2+nCO==wX(反应条件已省去,m、n、w为化学计量数)。如m:n=l:1且w=l,则有机物X可能是①HCHO②C2H5OH ③CH3COOH ④CH3CHO 中的
A. ①和② B. ①和③ C. ②和③ D. ①和④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年初天津连续出现了严重的雾霾天气,给人们的出行及身体造成了极大的危害.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
(1)利用钠碱循环法可脱除烟气中的SO2 . ①在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是 .
②吸收液吸收SO2的过程中,pH随n(SO32﹣):n(HSO3﹣)变化关系如下表:
n(SO32﹣):n(HSO3﹣) | 91:9 | 1:l | 9:91 |
pH | 8.2 | 7.2 | 6.2 |
由上表判断,NaHSO3溶液显性(填“酸”、“碱”或“中”),用化学平衡原理解释: .
③当吸收液的pH降至约为6时,需送至电解槽再生.再生示意图如下: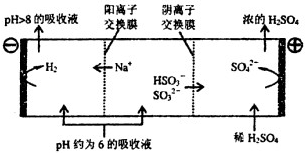
写出HSO3﹣在阳极放电的电极反应式: , 当阴极室中溶液pH升至8以上时,吸收液再生并循环利用.
(2)用CH4催化还原NOx可以消除氮氧化物的污染.例如: CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g);△H=﹣574kJmol﹣1
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g);△H=﹣1160kJmol﹣1
若用标准状况下4.48L CH4还原NO2至N2 , 整个过程中转移的电子总数为(阿伏伽德罗常数的值用NA表示),放出的热量为kJ.
(3)工业上合成氮所需氢气的制备过程中,其中的一步反应为:CO(g)+H2O(g) ![]() CO2(g)+H2(g);△H<0 一定条件下,将CO(g)与H2O(g)以体积比为1:2置于密闭容器中发生上述反应,达到平衡时测得CO(g)与H2O(g)体积比为1:6,则平衡常数K= .
CO2(g)+H2(g);△H<0 一定条件下,将CO(g)与H2O(g)以体积比为1:2置于密闭容器中发生上述反应,达到平衡时测得CO(g)与H2O(g)体积比为1:6,则平衡常数K= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质有以下转化关系: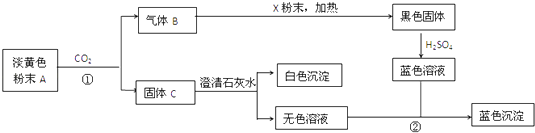
根据上图和实验现象,回答下列问题:(用化学式表示)
(1)A是 , B是 , C是 , X粉末是 .
(2)写出反应①的化学方程式 .
(3)写出反应②的离子方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com