
TiO2�ڹ�ҵ�������ճ�����������Ҫ��;��
��1����ҵ�����ѿ�ʯ��FeTiO3����FeO��Al2O3��SiO2�����ʣ�����������Ӧ�Ƶã�

���У�����ڷ�������Ҫ��ӦΪ��2H2SO4+FeTiO3 == TOSO4���������ѣ�+FeSO4+2H2O
�����ѿ�ʯʱ������Ũ����������Һ��������д���ù����з�����Ӧ�Ļ�ѧ����ʽ��________________��
������м��ȵ�Ŀ���ǣ���д����Ҫ�Ļ�ѧ����ʽ�����֣�: ��
��2����TiO2�Ʊ������ѵ�һ�ַ������Ƚ�TiO2��Cl2��C��Ӧ�õ�TiCl4������þ��ԭ�õ�Ti����������Ӧ���ڷ�����TiO2��s��+2Cl2��g�� TiCl4��1��+O2��g�� ��H��+151 kJ/mol�����Բ���ֱ����TiO2��Cl2��Ӧ�����Ȼ���Ӧ������ȡTiCl4����˵���жϸ÷�Ӧ���Է�����������_______�������Ȼ���Ӧ��ϵ�м���̼��Ӧ�ڸ�����������˳����������TiCl4��
TiCl4��1��+O2��g�� ��H��+151 kJ/mol�����Բ���ֱ����TiO2��Cl2��Ӧ�����Ȼ���Ӧ������ȡTiCl4����˵���жϸ÷�Ӧ���Է�����������_______�������Ȼ���Ӧ��ϵ�м���̼��Ӧ�ڸ�����������˳����������TiCl4��
��֪��C��s��+O2��g����CO2��g�� ��H= 394
kJ/mol��
394
kJ/mol��
��TiO2��s��+C��s��+2Cl2��g����TiCl4��1��+CO2��g�� ��H=________
�ӻ�ѧƽ��ĽǶȽ��ͣ����Ȼ���Ӧ��ϵ�м���̼ʱ���Ȼ���Ӧ��˳�����е�ԭ����_______________��
��3����ͼ��һ��Ⱦ������̫���ܵ�ص�ʾ��ͼ����ص�һ�����л�����Ⱦ�ϣ�S��Ϳ��TiO2����������Ƴɣ���һ�缫�ɵ��粣���Ʋ����ɣ�����з����ķ�ӦΪ��

TiO2/S TiO2/S*
������̬��
TiO2/S*
������̬��
TiO2/S*  TiO2/S+
+ e-
TiO2/S+
+ e-
I3-+2e- 3I-
3I-
2TiO2/S*+I3-  2TiO2/S + I3-
2TiO2/S + I3-
���й��ڸõ��������ȷ����
A.��ع���ʱ��I-�����ڶƲ����粣���缫�Ϸŵ�
B.��ع���ʱ���ǽ�̫����ת��Ϊ����
C.��صĵ������Һ��I-��I3- Ũ�Ȳ������
D.����жƲ����粣��Ϊ����
����14�֣���1��Al2O3 + 2NaOH��2NaAlO2 + H2O ��2�֣� SiO2 + 2NaOH��Na2SiO3 + H2O��2�֣�
TiOSO4��ˮ��TiOSO4
+ 2H2O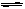 H2TiO3��+ H2SO4��һ�����ȷ�Ӧ�����ȴٽ�TiOSO4ˮ��������ȫ����2�֣�
��2���÷�Ӧ�ġ�H��0����S��0����Ӧ�����Է����У�2�֣�����243kJ/mol��2�֣���TiO2��s��+2Cl2��g��
H2TiO3��+ H2SO4��һ�����ȷ�Ӧ�����ȴٽ�TiOSO4ˮ��������ȫ����2�֣�
��2���÷�Ӧ�ġ�H��0����S��0����Ӧ�����Է����У�2�֣�����243kJ/mol��2�֣���TiO2��s��+2Cl2��g��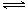 TiCl4��1��+O2��g�� ̼��������Ӧ����С�˲���O2��g����Ũ�ȣ�ƽ��������Ӧ�����ƶ���ʹ��Ӧ��˳�����У�1�֣� ��3��BCD��3�֣�
TiCl4��1��+O2��g�� ̼��������Ӧ����С�˲���O2��g����Ũ�ȣ�ƽ��������Ӧ�����ƶ���ʹ��Ӧ��˳�����У�1�֣� ��3��BCD��3�֣�
��������
�����������1�������ѿ�ʯ�к����������Ͷ������裬�����������������������������������������Ǿ��ܺ�����������Һ��Ӧ�����Ըù����з�����Ӧ�Ļ�ѧ����ʽ��Al2O3 + 2NaOH��2NaAlO2 + H2O��SiO2 + 2NaOH��Na2SiO3
+ H2O���������TiOSO4��ˮ����������Ĺ��̣�����TiOSO4��ˮ��TiOSO4
+ 2H2O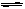 H2TiO3��+ H2SO4��һ�����ȷ�Ӧ����˼��ȵ�Ŀ���Ǵٽ�TiOSO4ˮ��������ȫ����2�����ݷ�Ӧ�ķ���ʽ��֪���÷�Ӧ�����ȵġ������С�Ŀ��淴Ӧ�����÷�Ӧ�ġ�H��0����S��0�� ���Է�Ӧ�����Է����У����ݷ�Ӧ��TiO2��s��+2Cl2��g��
H2TiO3��+ H2SO4��һ�����ȷ�Ӧ����˼��ȵ�Ŀ���Ǵٽ�TiOSO4ˮ��������ȫ����2�����ݷ�Ӧ�ķ���ʽ��֪���÷�Ӧ�����ȵġ������С�Ŀ��淴Ӧ�����÷�Ӧ�ġ�H��0����S��0�� ���Է�Ӧ�����Է����У����ݷ�Ӧ��TiO2��s��+2Cl2��g��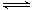 TiCl4��1��+O2��g���ͷ�Ӧ��C��s��+O2��g����CO2��g������ϸ�˹���ɿɣ��٣��ڼ��õ�TiO2��s��+C��s��+2Cl2��g����TiCl4��1��+CO2��g�� �����Ը÷�Ӧ�ķ�Ӧ�ȡ�H����151 kJ/mol��394 kJ/mol����243kJ/mol������̼��������Ӧ����С�˲���O2��g����Ũ�ȣ�ʹ���淴ӦTiO2��s��+2Cl2��g��
TiCl4��1��+O2��g���ͷ�Ӧ��C��s��+O2��g����CO2��g������ϸ�˹���ɿɣ��٣��ڼ��õ�TiO2��s��+C��s��+2Cl2��g����TiCl4��1��+CO2��g�� �����Ը÷�Ӧ�ķ�Ӧ�ȡ�H����151 kJ/mol��394 kJ/mol����243kJ/mol������̼��������Ӧ����С�˲���O2��g����Ũ�ȣ�ʹ���淴ӦTiO2��s��+2Cl2��g��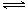 TiCl4��1��+O2��g��������Ӧ�����ƶ���������ʹ��Ӧ��˳�����С�
TiCl4��1��+O2��g��������Ӧ�����ƶ���������ʹ��Ӧ��˳�����С�
��3������ͼ�е��ӵ��ƶ������֪�������·�е����ɸ����������������뵼����TiO2��Ⱦ��Ϊԭ��صĸ��������缫Ϊԭ��ص������������ΪI3����I���Ļ���I3���������ϵõ��ӱ���ԭ��������ӦΪI3��+2e����3I������
A����ع���ʱ��I�������ڲ��缫�Ϸŵ磬����������Ӧ��A����ȷ��
B. �õ���ǽ�̫����ת��Ϊ���ܵ�װ�ã���B��ȷ��
C. ����֪��4����Ӧ�ϲ����õ��ܷ�ӦI3�� 3I�������Ե�صĵ������Һ��I-��I3-
Ũ�Ȳ�����٣�C��ȷ��
3I�������Ե�صĵ������Һ��I-��I3-
Ũ�Ȳ�����٣�C��ȷ��
D.����жƲ����粣��Ϊ������D��ȷ����ѡBCD��
���㣺�������ʵķ������ᴿ�����������ƽ��״̬��Ӱ�죻��Ӧ�Է��Ե��жϣ��绯ѧԭ�����й�Ӧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
TiO2�ڹ�ҵ�������ճ�����������Ҫ��;��
I����ҵ�����ѿ�ʯ��FeTiO3����FeO��Al2O3��SiO2�����ʣ�����������Ӧ�Ƶã�
���У�����ڷ����ķ�ӦΪ��2H2SO4��FeTiO3=TiOSO4��FeSO4��2H2O��
��1�������ѿ�ʯʱ���Ƿ���Ҫ��ȥ����FeO���� �����Ҫ������Ҫ������
��2�������ѿ�ʯʱ������Ũ����������Һ��������д���ù����з�����Ӧ�Ļ�ѧ����ʽ��
�� ��
II��TiO2��ͨ���������ַ����Ʊ������ѣ�
������һ���ǵ��TiO2�����Ti��ͬʱ����O2��������������TiO2��������ʯīΪ����������CaCl2Ϊ���Һ����̼�������۳ء�
��3��������Ӧ�ĵ缫��ӦʽΪ___________________________________��
��4�����������趨������۳��м���̼���ԭ����______________________��
�������������Ƚ�TiO2��Cl2��C��Ӧ�õ�TiCl4������þ��ԭ�õ�Ti����������Ӧ���ڷ�����
TiO2 (s)��2Cl2 (g)TiCl4(l)��O2(g) ��H=��151 kJ��mol��1
���Բ���ֱ���� TiO2 �� Cl2 ��Ӧ�����Ȼ���Ӧ������ȡTiCl4�������Ȼ���Ӧ��ϵ�м���̼��̼��������Ӧ������ϣ�ʹ�÷�Ӧ�ڸ�����������˳�����С�
��5����֪��C(s)��O2 (g) =CO2 (g) ��H=��394 kJ��mol��1������գ�
TiO2 (s)��C(s)��2Cl2 (g) = TiCl4 (l)��CO2(g) ��H= ______________
��6���ӻ�ѧƽ��ĽǶȽ��ͣ����Ȼ���Ӧ��ϵ�м���̼ʱ���Ȼ���Ӧ��˳�����е�ԭ��
��____________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010���Ĵ�ʡ�����и�����ǰģ�⿼�ԣ������ۺϣ���ѧ���� ���ͣ������
TiO2�ڹ�ҵ�������ճ�����������Ҫ��;��
I����ҵ�����ѿ�ʯ��FeTiO3����FeO��Al2O3��SiO2�����ʣ�����������Ӧ�Ƶã�

���У�����ڷ����ķ�ӦΪ��2H2SO4��FeTiO3=TiOSO4��FeSO4��2H2O��
��1�������ѿ�ʯʱ���Ƿ���Ҫ��ȥ����FeO���� �����Ҫ������Ҫ������
��2�������ѿ�ʯʱ������Ũ����������Һ��������д���ù����з�����Ӧ�Ļ�ѧ����ʽ��
�� ��
II��TiO2��ͨ���������ַ����Ʊ������ѣ�
������һ���ǵ��TiO2�����Ti��ͬʱ����O2��������������TiO2��������ʯīΪ����������CaCl2Ϊ���Һ����̼�������۳ء�
��3��������Ӧ�ĵ缫��ӦʽΪ___________________________________��
��4�����������趨������۳��м���̼���ԭ����______________________��
�������������Ƚ�TiO2��Cl2��C��Ӧ�õ�TiCl4������þ��ԭ�õ�Ti����������Ӧ���ڷ�����
TiO2 (s)��2Cl2 (g) TiCl4(l)��O2
(g) ��H=��151 kJ��mol��1
TiCl4(l)��O2
(g) ��H=��151 kJ��mol��1
���Բ���ֱ���� TiO2 �� Cl2 ��Ӧ�����Ȼ���Ӧ������ȡTiCl4�������Ȼ���Ӧ��ϵ�м���̼��̼��������Ӧ������ϣ�ʹ�÷�Ӧ�ڸ�����������˳�����С�
��5����֪��C(s)��O2 (g) = CO2 (g) ��H=��394 kJ��mol��1������գ�
TiO2 (s)��C (s)��2Cl2 (g) = TiCl4 (l)��CO2 (g) ��H= ______________
��6���ӻ�ѧƽ��ĽǶȽ��ͣ����Ȼ���Ӧ��ϵ�м���̼ʱ���Ȼ���Ӧ��˳�����е�ԭ��
��____________________________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com