
����Ŀ��������ͼ�ش��й����⡣
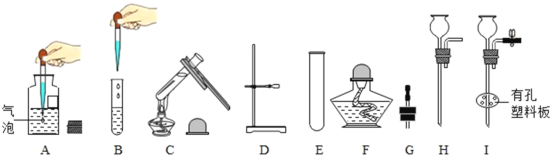
(1)����E������Ϊ___________��
(2)ͼA~C�dz���ʵ�����������������ȷ����___________������ţ�����ѡ��һ���д���IJ���д������������_________________________________________________________________________��
(3)ѡ������D~I�������ʵ�������
����KMnO4�Ʊ�O2��Ӧѡ����________������ţ����仯ѧ��Ӧ����ʽΪ_________________________________��
���ô���ʯ��ϡ���ᷴӦ�Ʊ�CO2��ʹ��Ӧ��ʱ������ֹͣ��Ӧѡ����___________���䷴Ӧ����ʽΪ______________________��
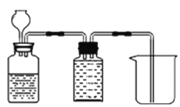
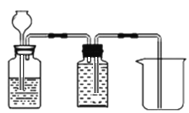
(4)��ͼ����п����ϡ���ᷴӦ�Ʊ�H2��������ˮ���ռ������ͼ��������____________��
���𰸡��Թ� B A ���ȼ�ѹ����ͷ�п������ٲ�����ȡҺ�壨��C,Һ����������ܳ����Թ��ݻ���1/3) DEFG 2KMnO4![]() K2MnO4+MnO2+O2
K2MnO4+MnO2+O2![]() E I CaCO3+2HCl=CaCl2+H2O+CO2
E I CaCO3+2HCl=CaCl2+H2O+CO2![]()
��������
��KMnO4�Ʊ�O2��ԭ��Ϊ2KMnO4![]() K2MnO4+MnO2+O2
K2MnO4+MnO2+O2![]() ����Ҫѡ����������ȡ�����װ�ã��ô���ʯ��ϡ���ᷴӦ�Ʊ�CO2Ӧѡ���Һ������װ�á�
����Ҫѡ����������ȡ�����װ�ã��ô���ʯ��ϡ���ᷴӦ�Ʊ�CO2Ӧѡ���Һ������װ�á�
��1������ͼ���֪������EΪ�Թܡ�
��2��A�����У�Ӧ�ȼ�����ͷ�еĿ������ٲ�����ȡҺ�壻C�����У�Һ����������ܳ����Թ��ݻ�������֮һ���ʲ�����ȷ����B��
��3������KMnO4�Ʊ�O2���䷢��װ��Ҫ�õ��Թܡ�����̨���ƾ��ơ�����Ƥ���ĵ��ܵȣ���ѡ������DEFG������������ȷֽ���������ء��������̺���������Ӧ����ʽΪ2KMnO4![]() K2MnO4+MnO2+O2
K2MnO4+MnO2+O2![]() ��
��
���ô���ʯ��ϡ���ᷴӦ�Ʊ�CO2��Ҫ�õ��������Թܡ�����©��������Ƥ���ĵ����ܣ�Ҫʹ��Ӧ��ʱ������ֹͣ��װ��ΪEI���رյ��ɼУ��Թ���ѹǿ����Һ��ᱻѹ�볤��©����ʹ��Һ���룻����ʯ��ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ���������ѧ����ʽΪCaCO3+2HCl=CaCl2+H2O+CO2![]() ��
��
��4����п����ϡ���ᷴӦ�Ʊ�H2��������ˮ���ռ�ʱ������©��Ҫ�嵽Һ�����£�����Ҫ�Ӷ̹ܽ���ˮ�ӳ��ܳ���װ��Ϊ ��
��


 ͬ��������ϰϵ�д�
ͬ��������ϰϵ�д� �ο�ͨ�γ̱�˼ά����������ѵ��ϵ�д�
�ο�ͨ�γ̱�˼ά����������ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������AlN���������¡�������������Ժõ��������ʣ����㷺Ӧ���ڵ��ӹ�ҵ���մɹ�ҵ��������һ�������£���������ͨ�����·�Ӧ�ϳɣ�Al2O3+N2+3C![]() 2AlN+3CO������������ȷ���ǣ� ��
2AlN+3CO������������ȷ���ǣ� ��
A���ڵ������ĺϳɷ�Ӧ�У�N2�ǻ�ԭ����Al2O3��������
B��������Ӧ��ÿ����2 mol AlN��N2�õ�3 mol����
C���������е�Ԫ�صĻ��ϼ�Ϊ��3
D���������������ڷ��Ӿ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ��������£�����ѡ����ʾ�����ʼ�ת������ʵ�ֵ���
A. NaHCO3(s)![]() Na2CO3(s)
Na2CO3(s)![]() NaOH(aq)
NaOH(aq)
B. Al(s)![]() NaAlO2(aq)
NaAlO2(aq)![]() Al(OH)3(s)
Al(OH)3(s)
C. AgNO3(aq)![]() [Ag(NH3)2]+(aq)
[Ag(NH3)2]+(aq)![]() Ag(s)
Ag(s)
D. Fe2O3(s)![]() Fe(s)
Fe(s)![]() FeCl3(aq)
FeCl3(aq)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��25��ʱ��0.1000mol��L-lCH3COOH��Һ��CH3COOH�ĵ����(��100%)ԼΪ1%�����¶��£���0.1000mol��L-l��ˮ�ζ�10.00mL0.1000mol��L-lCH3COOH��Һ����Һ��pH����Һ�ĵ�������(I)�Ĺ�ϵ��ͼ��ʾ������˵������ȷ���ǣ� ��
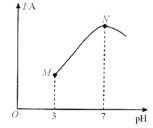
A.M���N�㣬ˮ�ĵ���̶�������
B.25��ʱ��CH3COOH �ĵ��볣��ԼΪ1.0��10-2
C.N����Һ�У�c(CH3COO-)>c(NH4+)
D.������20 mL��ˮʱ����Һ��c(CH3COO-)>c(NH4+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�ϵ��ȷ����
A. �е㣺�����飾2��2���������飾����
B. �ܶȣ�CCl4��H2O���ױ�
C. ������������ȼ�պ�O2�������飾��ϩ����Ȳ������
D. �����ʵ�������ȼ�պ�O2���������飾�������״�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̼��⼼��������ԭ���ԭ������������ˮ��һ�ֹ��գ�װ����ͼ��ʾ�����϶˿��ڹرգ��ɵõ�ǿ��ԭ�Ե�H��(��ԭ��);���϶˿��ڴ�������������ɵõ�ǿ�����Ե���OH���ǻ����ɻ�)������˵���������
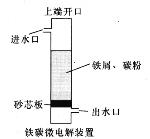
A. �����Ƿ��������������ĵ缫��Ӧʽ��ΪFe-2e��===Fe2+
B. ���������ʱ�������ĵ缫��ӦʽΪH++e��===H��
C. �������ʱ��ÿ����1mol��OH��2 mol���ӷ���ת��
D. �������в���(H2C2O4)����ˮʱ���϶˿���Ӧ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��µĺ����ܱ������У�����˵����ӦNH2COONH4(s)![]() 2NH3(g)+CO2(g)�ﵽƽ��״̬����
2NH3(g)+CO2(g)�ﵽƽ��״̬����
A. ���������ܶȲ��ٷ����仯
B. �������������ʵ������ٷ����仯
C. ��������ƽ����Է����������ٷ����仯
D. ��������ѹǿ���ٷ����仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ����ʵ�ó��Ľ�����ȷ���ǣ�������
A.��SiO2������ˮ��Ӧ����H2SiO3����֪SiO2��������������
B.��SiO2��2C![]() Si��2CO������֪̼�ķǽ����Դ��ڹ�
Si��2CO������֪̼�ķǽ����Դ��ڹ�
C.CO2ͨ��Na2SiO3��Һ������ɫ��������֪����H2CO3>H2SiO3
D.SiO2��NaOH��Һ��Ӧ��Ҳ��������ᷴӦ����SiO2Ϊ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£�ͨ�����з�Ӧ��ʵ��ȼú��������Ļ��գ�SO2(g)+2CO(g)![]() 2CO2(g)+S(s) ��H<0������Ӧ�ں��ݵ��ܱ������н��У������й�˵����ȷ���ǣ� ��
2CO2(g)+S(s) ��H<0������Ӧ�ں��ݵ��ܱ������н��У������й�˵����ȷ���ǣ� ��
A. ƽ��ǰ�����ŷ�Ӧ�Ľ��У�������ѹǿʼ�ղ���
B. ƽ��ʱ���������¶ȣ�CO�����������ƽ�ⳣ����С
C. ƽ��ʱ�������������䣬�����CO2������Ӧ���ʼӿ�
D. ƽ��ʱ��v����SO2��=2v����CO��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com