
科目:高中化学 来源: 题型:
短周期金属元素甲~戊在元素周期表的相对位置如表所示。下列判断正确的是
A.氢氧化物碱性:丙>丁>戊
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
B.金属性:甲>丙
C.原子半径:丙<丁<戊
D.最外层电子数:甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
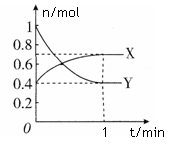
在一定温度下,体积为2 L的密闭容器中,NO2和N2O4之间发生反应:2NO2 (g) (红棕色) N2O4(g) (无色),如图所示。
N2O4(g) (无色),如图所示。
(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。
(2)若升高温度,则v(正) ,v(逆) 。(填“加快”或“减慢”)。
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=18 mol/(L·min),乙中v(N2O4)=0.2 mol/(L·s),则 中反应更快。
(4)在0到1 min中内用X表示该反应的速率是 ,该反应达限度时,Y的转化率 ,反应开始时与反应达平衡状态时的压强之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
pH=2的A、B两种酸溶液各lmL,分别加水稀释到1000 mL,其溶液的pH与溶液体积(V)的关系如图所示,则下列说法正确的是( )
A.A、B两种酸溶液物质的量浓度一定相等
B.稀释后A酸溶液的酸性比B酸溶液强
C.a=5时,A是弱酸,B是强酸
D.若A、B都是弱酸,则5>a>2

查看答案和解析>>
科目:高中化学 来源: 题型:
按以下步骤可从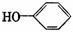 合成
合成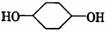 (部分试剂和反应条件已去).
(部分试剂和反应条件已去).

请回答下列问题:
(1)B、F的结构简式为:B F 。
(2)反应①~⑦中属于消去反应的是 (填代号)。
(3)根据反应 ,写出在同样条件下
,写出在同样条件下
CH2=CH—CH=CH2与等物质的量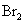 发生加成反应的化学方程式: 。
发生加成反应的化学方程式: 。
(4)写出第④步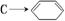 的化学方程式(有机物写结构简式,注明反应条件). 。
的化学方程式(有机物写结构简式,注明反应条件). 。
(5)A—G这七种有机物分子中含有手性碳原子的是(填序号) 。
(注:碳原子连有四个不同的原子或原子团即为手性碳原子)
(6)核磁共振谱是测定有机物分子结构最有用的工具之一。在有机物分子中,不同位置的氢原子在质子核磁共振谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目。例如:乙醛的PMR谱中有2个信号峰,其强度之比为3∶1。则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1∶1∶2的是 。
A.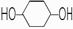 B.
B.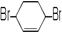 C.
C.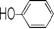 D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
由乙烯推测丙烯(CH2=CH-CH3)与溴水反应时,反应产物是( )
A.CH2Br—CH2—CH2Br B.CH3-CBr2-CH3
C.CH3-CH2-CHBr2 D.CH3—CHBr—CH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
在20℃时,某气态烃与氧气混合装入密闭容器中点燃爆炸后,恢复到20℃,此时容器内气体的压强为反应前的一半,经氢氧化钠溶液吸收后,容器内几乎成真空,此烃的分子式可能是( )
A.CH4 B.C2H6 C.C3H8 D.C2H4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关元素的性质及其递变规律正确的是
A.IA族与ⅦA族元素间可形成共价化合物或离子化合物
B.第二周期元素从左到右,最高正价从+1递增到+7
C.同主族元素的简单阴离子还原性越强,对应氢化物的稳定性越强
D.同周期金属元素的化合价越高,其原子失电子能力越强
查看答案和解析>>
科目:高中化学 来源: 题型:
在氯化铁、氯化铜和盐酸的混合溶液中加入铁粉,待反应结束后,所剩余的固体滤出后能被磁铁吸引,则反应后溶液中存在较多的阳离子是( )
A.Cu2+ B.Fe3+
C.Fe2+ D.H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com