
下列化合物中,阴、阳离子都具有与氖原子相同的电子层结构的是( )
A.KCl B.Na2S C.MgO D.Al2O3
科目:高中化学 来源: 题型:
| 元素 | 钠 | 镁 | 铝 | 硅 |
| 电负性 | 0.9 | 1.2 | x | 1.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 工业上电解制碱的技术是用离子交换膜法,主要原料是饱和食盐水.下图为离子交换膜法电解原理示意图:请回答下列问题:
工业上电解制碱的技术是用离子交换膜法,主要原料是饱和食盐水.下图为离子交换膜法电解原理示意图:请回答下列问题:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
①元素的原子序数按A、B、C、D、E依次增大,原子半径按D、E、B、C、A顺序依次减小;
②A、D同主族,A是所有元素中原子半径最小的元素;?
③B、D、E三者的最高价氧化物对应的水化物依次为甲、乙、丙,它们两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素;?
④B、E两种元素原子最外层电子数之和等于A、C、D三种元素原子最外层电子数之和。
请填写下列空白:?
(1)D2C2的电子式 。?
(2)1 mol E单质与足量乙的溶液反应,能生产 mol A2气体。并写出其反应的离子方程式 。
(3)写出下列溶液反应的离子方程式:?
乙+丙: 。?
(4)化合物BA3与BC在加热和有催化剂存在的条件下能发生反应,生成两种无毒物质,其反应的化学方程式为 。?
(5)以石墨为电极,电解乙的溶液400 mL,当电路中通过a mol电子时,阴、阳两极共产生气体 L(标准状况),溶液中c(OH-) (填“增大”“减小”或“不变”)。?
查看答案和解析>>
科目:高中化学 来源:2012届河北省衡水中学高三下学期二调考试理综试卷(带解析) 题型:填空题
(Ⅰ)氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用。
(1)一定温度下,在1L容积恒定的密闭容器中充入2mol N2和8mol H2并发生反应。10min达平衡,测得氨气的浓度为0.4mol/L,此时氮气的转化率为 。
(2)下图是1mol NO2(g)和1mol CO(g)反应生成1mol CO2(g)和1mol NO(g)过程中能量变化示意图,请写出该反应的热化学方程式 。
(3)NH3(g)燃烧的方程式4NH3(g)+7O2(g)==4NO2(g)+6H2O(l),
已知:2H2(g)+O2(g)==2H2O(l) △H=" -483.6" kJ/mol
N2(g)+2O2(g)==2NO2 (g) △H="+67.8" kJ/mol
N2(g)+3H2(g)==2NH3 (g) △H="-92.0" kJ/mol
请计算NH3 (g)的燃烧热 。
| 温度[来源:学§科§网] | 平衡浓度/ (mol L-1)[来源:学*科*网Z*X*X*K] | |
| c(NH3) | c(CO2) | |
| T1 | 0.1 | |
| T2 | | 0.1 |
 2NH3(g)+CO2(g) 在不同温度下,该反应平衡状态部分数据见右表。下列说法正确的是
2NH3(g)+CO2(g) 在不同温度下,该反应平衡状态部分数据见右表。下列说法正确的是 | 成分 | 含量/(mg L-1) | 成分 | 含量/(mg L-1) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Br- | 64 |
| Mg2+ | 1272 | | |
 电渗析法淡化海水示意图如下图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过。
电渗析法淡化海水示意图如下图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河南省原名校高三下学期第二次联考理综化学试卷(解析版) 题型:推断题
A-J是中学化学中常见的几种物质,它们之间的转化关系如图所示。已知常温下A为固体单质,B为淡黄色粉末, C、F、I为气态单质,E在常温下为液体,且E可由C、F合成,J可用作杀菌消毒剂。回答下列问题:
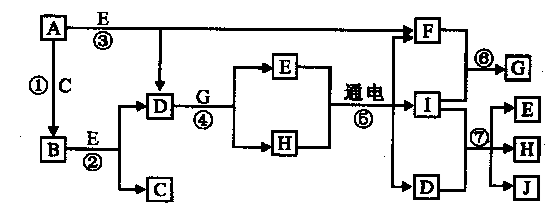
(1)B中阴离子的电子式为 ,与E组成元素相同的化合物的结构式为 。
(2)已知D与G反应生成ImolE放出的热量为aKJ,请写出表示D与H2SO4中和热的热化学方程式 。
(3)向FeCl2溶液中加入大量固体B,写出反应离子方程式 。
(4)常温下以Pt为电极电解滴加有少量酚酞的H饱和溶液2L,则在 (填“阴或阳”)极附近溶液由无色变为红色,若用F、C组成电池(熔融K2CO3做电解质)供电,电池的负极反应式为 ,正极反应式为 ,电解过程中,忽略溶液体积变化,则当溶液的PH=13时,负极消耗气体的体积在标况下为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com