
查文献知,CH3COOH、H3PO3(二元酸)、H3PO4三种酸所有的逐级电离常数如下:
| 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
| CH3COOH | 1.8×10-5 | H3PO4 | K1=7.1×10-3 |
| H3PO3 | K1=3.7×10-2 | K2=6.2×10-8 | |
| K2 =2.9×10-7 | K3=4.5×10-13 |
用化学用语回答下列问题:
(1)上述三种酸中,酸性最强的是 ;
(2)常温下,在NaH2PO3稀溶液中:c(H3PO3) < c(HPO32-),则该溶液pH_______7;(填“>”“<”或“=”)
(3)等温度、等浓度的NaH2PO4溶液与Na2HPO4溶液比较,c(H3PO4)较大的是:___ __;
(4)25℃时,浓度均为0.01 mol/L 的CH3COONa、Na2HPO3、Na3PO4溶液,pH最大的是:_________________;
(5)在NaH2PO3溶液中,粒子间存在等量关系:c(H3PO3)+_____________= c(Na+)。(用溶液中其它粒子浓度补充完整)
科目:高中化学 来源: 题型:
工业上研究燃料脱硫的过程中,涉及如下反应:
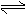 CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g),K1,△H1= 218.4 kJ·mol-l(反应I)
CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g),K1,△H1= 218.4 kJ·mol-l(反应I)

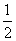 CaSO4(s)+2CO(g)
CaSO4(s)+2CO(g) 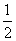 CaS(s)+2CO2(g),K2,△H2= -87.8 kJ·mol-l(反应II)
CaS(s)+2CO2(g),K2,△H2= -87.8 kJ·mol-l(反应II)
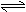 (1)反应CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g)的△H= ;平衡常数K= (用K1,K2表示)。
(1)反应CaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g)的△H= ;平衡常数K= (用K1,K2表示)。
(2)某温度下在一密闭容器中若只发生反应I,测得数据如下:

前100 s 内v(SO2)= mo1·L-1·s-l,平衡时CO的转化率为 。
(3)若只研究反应II,在不同条件下其反应能量变化如下图所示:图中曲线a到曲线b的措施是________,恒温恒容时,下列说法能说明反应Ⅱ到达平衡状态的是____ 。

A.体系中气体的平均摩尔质量不再改变
B.v(CO)=v(CO2)
C.CO的转化率达到了最大限度
D.体系内气体压强不再发生变化
(4)某科研小组研究在其它条件不变的情况下,改变起始一氧化碳物质的量[用n(CO)表示]对CaO(s)+3CO(g)+SO2(g)
 CaS(s)+3CO2(g)反应的影响,实验结果如右图所示(图中T表示温度):
CaS(s)+3CO2(g)反应的影响,实验结果如右图所示(图中T表示温度):
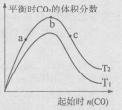
①比较在a、b、c三点所处的平衡状态中,反应物SO2的转化率最高的是____ 。
②图像中T2 T1(填“高于”、“低于”、“等于”或“无法确定”):判断的理由是____ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的值。下列叙述正确的是
A.常温常压下,46g NO2与N2O4的混合气体中含有的分子总数为NA
B.0.1mol乙烯和乙醇的混合物完全燃烧所消耗O2的分子数为0.3NA
C.25。C时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.1 NA
D.一定量的钠与8g氧气作用,若两者均无剩余,转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中错误的是( )
A. 盐类都能水解
B. 配制FeCl3溶液,为了抑制水解,常加入盐酸
C. 盐类的水解反应,通常是吸热反应
D. 盐类水解是指组成盐的离子跟水电离出来的H+或OH—生成弱电解质的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
一定质量的无水乙醇完全燃烧时放出的热量为Q,它所生成的CO2用过量的饱和石灰水完全吸收可得100gCaCO3沉淀,则完全燃烧1mol无水乙醇时放出的热量是( )
A.0.5Q B. Q C. 2Q D.5Q
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4NH3(g)+5O2(g)===4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加
了0.45 mol,则此反应的速率v(X)(反应物的消耗速率或产物的生成速率)可表示为( )
A.v(NH3)=0.010 mol·L-1·s-1 B.v(O2)=0.001 0 mol·L-1·s-1
C.v(NO)=0.001 0 mol·L-1·s-1 D.v(H2O)=0.045 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
将等物质的量的A和B混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)xC(g)+2D(g),经5 分
钟后,测得 D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,C的平均反应速率是0.1 mol·L-1·min-1。A在5
D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,C的平均反应速率是0.1 mol·L-1·min-1。A在5
min末的浓度是________,B的平均反应速率是________,D的平均反应速率是________,x的值是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如下图所示。下列判断正确的是
A.在0~50 min之间,pH=2和pH=7时R的降解
百分率相等
B.溶液酸性越强,R的降解速率越小
C.R的起始浓度越小,降解速率越大
D.在20~25 min之间, pH=10时R的平均降解速率为
0.04 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
I. 下面列出了几组物质或粒子,请将合适的组号填写在空格上。
①金刚石与“足球烯”(C60)
②CH3CH2CH2CH(C2H5)CH3 和 CH3CH2CH2CH(CH3)C2H5
③235U、238U ④氧气(O2)与臭氧(O3)
⑤乙醇(CH3CH2OH)和甲醚(CH3OCH3) ⑥淀粉和纤维素
⑦ 
(1)是同素异形体的是 ,(填序号,下同)
(2)是同位素的是 ,
(3)是同分异构体的是 ,
(4)是同一物质的是 。
II. 下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤C2H6 ⑥MgF2 ⑦HNO3
(1)只由离子键构成的物质是______________(填序号,下同)(2)由离子键和非极性键构成的物质是______________(3)由极性键和非极性键构成的物质是______________
III. 提纯下列物质(括号内的物质是杂质),请将所选用的除杂试剂和分离方法(填字母或者序号)填入对应的空格中(若不选,填“无”)
除杂试剂:A. 盐酸 B. 酸性高锰酸钾 C. 氢氧化钠溶液 D. (浓)溴水
E. H2(催化剂) F. CaO G. NaCl
分离方法:① 蒸馏 ② 分液 ③ 洗气 ④ 过滤
| 被提纯的物质 | 除杂试剂 | 分离方法 | |
| (1) | 酒精(水) | ||
| (2) | 乙烷(乙烯) | ||
| (3) | 硬脂酸钠溶液(甘油) | ||
| (4) | 苯(苯酚) | ||
| (5) | SiO2(Al2O3) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com