
| A. | 若温度不变将容器的容积增大1倍,达到新平衡时A的浓度变为原来的0.55 倍,则m+n<p+q | |
| B. | 若升高平衡体系的温度,达到新平衡时A 的浓度变为原来的0.55 倍,说明该反应△H<0 | |
| C. | 若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n | |
| D. | 若平衡后同时增大A、B的浓度,则A、B的转化率一定都减小 |
分析 A.若温度不变,将容器的体积增大1倍,若平衡不移动,A的浓度为原来的一半,而此时A的浓度为原来的0.55倍,则增大体积平衡逆向移动;
B、若升高平衡体系的温度,达到新平衡时A 的浓度减小,平衡正向移动,向着吸热反应移动;
C、当反应物的物质的量之比等于系数值比时,则达到化学平衡时,反应物的转化率是相等的;
D、若平衡后同时增大A、B的浓度,体积不变,相当于增加压强,平衡正向移动.
解答 解:A.若温度不变,将容器的体积增大1倍,若平衡不移动,A的浓度为原来的一半,而此时A的浓度为原来的0.52倍,则增大体积平衡逆向移动,即增大体积,压强减小,平衡向气体体积增大的方向移动,所以m+n>p+q,故A错误;
B、若升高平衡体系的温度,达到新平衡时A 的浓度减小,平衡正向移动,即向着吸热反应移动,说明该反应△H>0,故B错误;
C、当反应物的物质的量之比等于系数值比时,则达到化学平衡时,反应物的转化率是相等的,故C正确;
D、若平衡后同时增大A、B的浓度,则A、B的转化率不一定减小,故D错误.
故选C.
点评 本题考查化学平衡的影响因素,注意对于反应前后气体体积不变的反应压强改变不会引起平衡移动,把握化学计量数的关系、压强对平衡的影响为解答的关键,选项C为易错点,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 已知:Ⅰ:对于反应:H2(g)+Cl2(s)═2HCl (g)△H=-a kJ/mol, Ⅱ:  且a、b、c均大于零,则断开1molH-Cl键所需的能量为-a-b-c | |
| B. | 若2C(s)+O2(g)═2CO(g)△H=-221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol | |
| C. | 需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 | |
| D. | 如图可表示水分解过程中的能量变化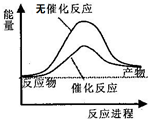 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 50g | 20g | 20g | 10g | 5g |
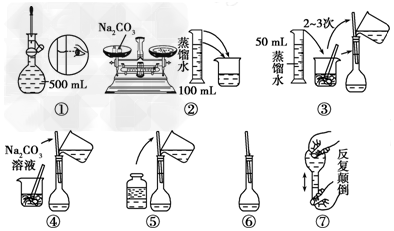
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2和CO对容器产生的压强之比是7:11 | |
| B. | CO2和CO的密度之比是11:7 | |
| C. | CO2和CO的分子数相等 | |
| D. | CO2和CO的氧原子个数比是22:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0g | B. | 2.0g | C. | 2.5g | D. | 3.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH=CH-CH3+Br2$→_{△}^{催化剂}$ | |
| B. | CH2=CH-CH2CH3+HCl | |
| C. | CH3-CH=CH2+H2O $→_{加热、加压}^{催化剂}$ | |
| D. | CH3CH3+Cl2$\stackrel{光照}{→}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学式 | CH3COOH | HCN |
| 电离平衡常数 | 1.8×10-5 | 4.9×10-10 |
| A. | 体积和pH相同的CH3COOH溶液与HCN溶液,分别与足量的Fe反应,HCN溶液产生的H2更多 | |
| B. | 体积和pH相同的CH3COOH溶液与HCN溶液,中和NaOH溶液所消耗NaOH的物质的量相同 | |
| C. | amol•L-1HCN溶液加水稀释后,电离平衡常数减小,加入KCN晶体后,电离平衡常数增大 | |
| D. | 25℃时,在等浓度的CH3COOH溶液与HCN溶液中,水的电离程度前者大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有12 mol KI 被氧化 | B. | 转移11 mol电子 | ||
| C. | 生成CuI 382g | D. | I2只是氧化产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 实验室要配制0.lmol/LNaOH溶液400mL,需称取NaOH 固体1.6g | |
| B. | 焰火的五彩缤纷是某些金属元素化学性质的展现 | |
| C. | Al2O3熔点很高,可用作耐火材料 | |
| D. | 纯锌和铁相连接后,插入同一稀盐酸中,锌极上发生氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com