
 R2Cu(�л���)+2H��(ˮ��)������л��࣬�����м���һ��Ũ�ȵ����ᣬʹCu2+���������� �����������ͭ��Һ�Ƶý���ͭ��
R2Cu(�л���)+2H��(ˮ��)������л��࣬�����м���һ��Ũ�ȵ����ᣬʹCu2+���������� �����������ͭ��Һ�Ƶý���ͭ�� R2Cu(�л���)+ 2H��(ˮ��)�����ƶ���Cu2+����ˮ��������� ��2�֣� ��5��c(H+)��c(SO42�C)��c(Cu2+)��c(OH�C) ��2�֣�
R2Cu(�л���)+ 2H��(ˮ��)�����ƶ���Cu2+����ˮ��������� ��2�֣� ��5��c(H+)��c(SO42�C)��c(Cu2+)��c(OH�C) ��2�֣� R2Cu(�л���)+ 2H��(ˮ��)�����ƶ���Cu2+����ˮ�����������
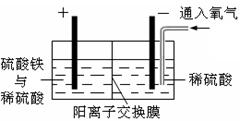
R2Cu(�л���)+ 2H��(ˮ��)�����ƶ���Cu2+����ˮ����������� 2Cu��2H2SO4��O2����֪����Һ�л�����0.05mol���ᡣ����ͭ����ˮ�⣬����Һ������Ũ�ȴ�С˳���ǣ�c(H+)��c(SO42�C)��c(Cu2+)��c(OH�C)��
2Cu��2H2SO4��O2����֪����Һ�л�����0.05mol���ᡣ����ͭ����ˮ�⣬����Һ������Ũ�ȴ�С˳���ǣ�c(H+)��c(SO42�C)��c(Cu2+)��c(OH�C)��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
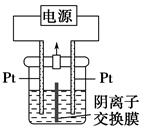
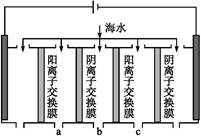
| A���Ҳ���ĵ缫��Ӧʽ��2H2O��2e��=H2����2OH�� |
| B��������ʱ���Ҳ���Һ�к�IO3�� |
C�������ڷ�����Ӧ���ܻ�ѧ����ʽ��KI��3H2O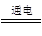 KIO3��3H2�� KIO3��3H2�� |
| D������������ӽ���Ĥ���������ӽ���Ĥ�������ڷ������ܻ�ѧ��Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| �ɷ� | Na+ | K+ | Ca2+ | Mg2+ | Cl- | S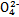 | HC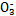 |
| ����/(mg��L-1) | 9 360 | 83 | 200 | 1 100 | 16 000 | 1 200 | 118 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
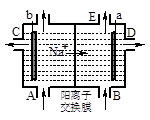
A��a���ĵ缫��ӦʽΪ��2 H++ 2 e H2 �� H2 �� |
| B��D�ڵ�������NaOH��Һ |
| C��Ũ��ˮ��A��ע�� |
| D��C�ڵ�������NaOH��NaCl�Ļ����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
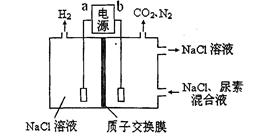
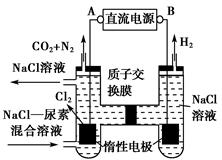
| A����Դ������Ϊb |
| B�����ر������Ļ�ѧ����ʽΪCO(NH2)2��3Cl2��H2O��N2��CO2��6HCl |
| C������������������Һ����ǰ���pH���� |
| D�������ռ�������4.48 L����״����ʱ��������������Ϊ6.0 g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
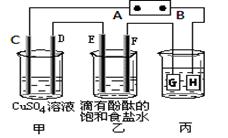
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ֻ��Cl2 | B��ֻ��O2 | C��ֻ��H2 | D������Cl2����O2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com