
| A. | X>Z>Y>W | B. | Z>W>X>Y | C. | Z>X>Y>W | D. | Z>Y>X>W |
分析 据同一化学反应中,还原剂的还原性大于还原产物的还原性,原电池的负极金属活泼性强于正极金属的活泼性,据此分析X、Y、Z、W的还原性强.
解答 解:①X+Y2+=X2++Y,X作还原剂,Y是还原产物,所以X的还原性大于Y的还原性;
②Z+H2O=Z(OH)2+H2↑,Z能与水反应作还原剂,所以Z的还原性最强;z作还原剂,氢气是还原产物,所以Z的还原性大于氢气的还原性;
③由Y、W电极组成的电池,电极反应为W2++2e-=W、Y-2e-=Y2+,Y是还原剂,W是还原产物,所以Y的还原性大于W的还原性;
所以X、Y、Z、W的还原性由强到弱的顺序为Z>X>Y>W.
故选C.
点评 本题考查了还原性强弱的比较,难度不大,明确同一化学反应中,还原剂的还原性大于还原产物的还原性,氧化剂的氧化性大于氧化产物的氧化性.


科目:高中化学 来源: 题型:选择题
| A. | H2(g)+Br2(g)?2HBr(g) 恒温、恒容下,反应体系中气体的颜色保持不变 | |
| B. | 2NO2(g)?N2O4(g) 恒温、恒容下,反应体系中气体的压强保持不变 | |
| C. | CaCO3(s)?CO2(g)+CaO(s) 恒温、恒容下,反应体系中气体的密度保持不变 | |
| D. | 3H2(g)+N2(g)?2NH3(g) 反应体系中H2与N2的物质的量之比保持3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
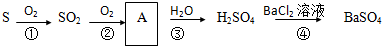
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A原子的最外层电子数比B原子的最外层电子数少 | |
| B. | A原子的电子层数比B原子多 | |
| C. | 1 mol A从酸中置换出H2比1 mol B多 | |
| D. | 常温下,A能从酸中置换出氢气,而B不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最高正化合价:F>O>N>C>Al | B. | 离子半径:F->O2->Na+>Al3+ | ||
| C. | 热稳定性:PH3<H2S<HCl<HF | D. | 碱性强弱:NaOH>Mg(OH)2>Al(OH)3>KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Al、Cl的原子半径依次减小,Na+、Al3+、Cl-的离子半径也依次减小 | |
| B. | 在第ⅥA族元素的氢化物(H2R)中,热稳定性最强的是H2O | |
| C. | 第二周期元素的最高正化合价都等于其原子的最外层电子数 | |
| D. | 非金属元素的非金属性越强,其氧化物对应水化物的酸性也一定越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O=2H++Cl-+ClO- | |
| B. | 过氧化钠反应生成NaOH和H2:Na2O2+H2O=2Na++2OH-+O2↑ | |
| C. | 酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+=I2+3H2O | |
| D. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应过程的热效应称为燃烧热 | |
| B. | 该过程是吸热反应 | |
| C. | 生成物的总能量等于反应物的总能量 | |
| D. | 化学能转变成热能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com