
分析 根据n=cV计算出硫酸铝的物质的量,然后根据硫酸铝的化学式组成计算出铝离子、硫酸根离子的物质的量,最后根据N=nNA计算出硫酸根离子的数目.
解答 解:100mL 1mol•L-1Al2(SO4)3溶液中含有硫酸铝的物质的量为:1mol/L×0.1L=0.1mol,0.1mol Al2(SO4)3中含有硫酸根离子的物质的量为:0.1mol×3=0.3mol,含有铝离子的物质的量为:0.1mol×2=0.2mol;含有硫酸根离子的数目为0.3NA或1.806×1023,
故答案为:0.3NA或1.806×1023;0.2.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、阿伏伽德罗常数之间的关系即可解答,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:实验题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
| 编号 | C(H2)mol/L | C(CO)mol/L |
| 甲 | 2 | 1 |
| 乙 | 1 | 2 |
| 丙 | 1 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡膳食就是各种食物都要吃 | |
| B. | 摄入食物中的营养素种类齐全,数量充足,比例适当且与人体的需要的保持平衡才是合理的膳食结构 | |
| C. | 淀粉、油脂、蛋白质为人体提供热能,所以只要这三种摄入量足够就可以了 | |
| D. | 麦芽糖不可以水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可溶性铁盐或铝盐可用于水的净化 | |
| B. | 电解MgCl2溶液可制得金属镁 | |
| C. | 在海轮的外壳镶上锌块,可减缓船体的腐蚀速率 | |
| D. | “开发利用新能源”、“汽车尾气催化净化”都能提高空气质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴苯中的溴(苯) | |
| B. | MgCl2酸性溶液中少量的FeCl3(Mg(OH)2) | |
| C. | 硝基苯中的苯(硝酸) | |
| D. | 甲烷中的乙烯(酸性高锰酸钾溶液) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
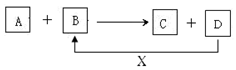 A、B、C、D、X均为中学化学常见的物质.它们之间存在如图所示转化关系.(图中反应条件略去)填写下列空白.
A、B、C、D、X均为中学化学常见的物质.它们之间存在如图所示转化关系.(图中反应条件略去)填写下列空白.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com