
A.a+b<c+d,ΔH<0 B.a+b>c+d,ΔH<0
C.a+b<c+d,ΔH>0 D.a+b=c+d,ΔH<0
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器编号 | 起始浓度mol/L | 平衡时的浓度mol/L | 平衡时放出的热量/KJ | |
| I2 | H2 | HI | ||
| 甲 | 0.01 | 0.01 | 0.004 | Q1 |
| 乙 | 0.02 | 0.02 | a | Q2 |
| A、平衡时,乙中颜色更深,a>0.008 | ||
B、平衡时,放出的热量:Q1=
| ||
| C、该温度下,该反应的平衡常数K=4 | ||
| D、平衡后,向甲中再充入0.004mol HI气体,再次达到平衡时HI的百分含量不变 |
查看答案和解析>>
科目:高中化学 来源:山东省临沂高新区实验中学2008-2009学年高三12月月考化学试题 人教版 人教版 题型:022
合成氨工业对化学工业和国防工业具有重要意义.
(1)常温下氨气极易溶于水,其水溶液可以导电.
①用方程式表示氨气溶于水的过程中存在的可逆过程__________________
②氨水中水电离出的c(OH-)________10-7 mol/L(填写“>”、“<”或“=”)
③将相同体积、相同物质的量浓度的氨水和盐酸混合后,溶液中离子浓度由大到依次为________.
(2)氨气具有还原性,在铜的催化作用下,氨气和氟气反应生成A和B.A为铵盐,B在标准状况下为气态.在此反应中,若每反应1体积氨气,同时反应0.75体积氟气;若每反应8.96 L氨气(标准状况),同时生成0.3 mol A.
①写出氨气和氟气反应的化学方程式________;
②在标准状况下,每生成1 mol B,转移电子的物质的量为________mol.
(3)Ⅰ在某压强恒定的密闭容器中加入2 mol N2和4 mol H2,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ/mol
2NH3(g) ΔH=-92.4 kJ/mol
达到平衡时,体积为反应前的三分之二.求:
①达到平衡时,N2的转化率为________.
②若向该容器中加入a mol N2、b mol H2、c mol NH3,且a、b、c均>0,在相同条件下达到平衡时,混合物中各组分的物质的量与上述平衡相同.试比较反应放出的能量:①________②(填“>”、“<”或“=”)
Ⅱ若将2 mol N2和4 mol H2放入起始体积相同的恒容容器中,在与Ⅰ相同的温度下达到平衡.
③试比较平衡时NH3的浓度:Ⅰ________Ⅱ(填“>”、“<”或“=”).
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工业对化学工业和国防工业具有重要意义。
(1)常温下氨气极易溶于水,其水溶液可以导电。
①用方程式表示氨气溶于水的过程中存在的可逆过程
_______________________________________________________________
②氨水中水电离出的![]() (填写“>”、“<”或“=”)
(填写“>”、“<”或“=”)
③将相同体积、相同物质的量浓度的氨水和盐酸混合后,溶液中离子浓度由大到小依次为__________________。
(2)氨气具有还原性,在铜的催化作用下,氨气和氟气反应生成A和B。A为铵盐,B在标准状况下为气态。在此反应中,若每反应1体积氨气,同时反应0.75体积氟气;若每反应8.96L氨气(标准状况),同时生成0.3molA。
①写出氨气和氟气反应的化学方程式___________________________;
②在标准状况下,每生成1mol B,转移电子的物质的量为_________mol。
(3)I 在某压强恒定的密闭容器中加入2mol N2和4 mol H2,发生如下反应:
N2(g)+3H2 (g)![]() NH3(g)
NH3(g)![]()
达到平衡时,体积为反应前的三分之二。求:
①达到平衡时,N2的转化率为_________。
②若向该容器中加入amol N2、b mol H2、c mol NH3,且a、b、c均>0,在相同条件下达到平衡时,混合物中各组分的物质的量与上述平衡相同。试比较反应放出的能量:
①_________②(填“>”、“<”或“=”)。
Ⅱ 若将2 mol N2和4 mol H2放入起始体积相同的恒容容器中,在与I相同的温度下达到平衡。
③试比较平衡时NH3的浓度I_________Ⅱ (填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在容积为1L的密闭容器中发生可逆反映:![]() 。在1000℃时,
。在1000℃时,![]() 的平衡转化率
的平衡转化率![]() 与体系总压强
与体系总压强![]() 的关系如图所示:
的关系如图所示:
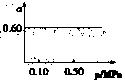
(1)写出该反应的平衡常数表达式K= ;当反应达到平衡后,再向容器中加入铁粉和水蒸气,则K ;升高温度,则K (后两空填“增大”“减小”或“不变”)。
(2)在1000℃时,若向上述容器中加入0.80mol铁粉和1.00mol水蒸气,达到平衡是,容器中![]() = 。
= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com