
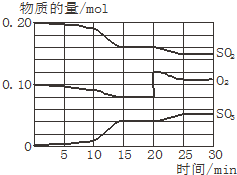
 一定条件下,将SO2和O2充入一密闭容器中,发生如下反应:2SO2(g)+O2(g)?2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如图所示:回答下列问题:
一定条件下,将SO2和O2充入一密闭容器中,发生如下反应:2SO2(g)+O2(g)?2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如图所示:回答下列问题:

 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
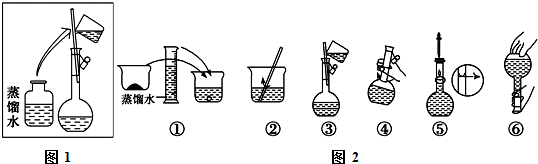
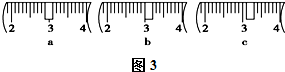
| a | b | c | d | e | |
| 砝码大小/g | 100 | 50 | 20 | 10 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若起始时加入容器的只有反应物X、Y,则起始加入的X、Y的物质的量之比一定是2:3 |
| B、若起始时加入容器的有X、Y、Z,则起始时加入的X、Y的物质的量之比一定是2:3,而Z的物质的量一定小于1.2mol |
| C、达到平衡状态时,Z的浓度可能是0.1mol/L也可能是0.6mol/L |
| D、达到平衡状态时,X的浓度可能是0.1mol/L也可能是0.4moL/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 |
| B、原子核外M层上有2个电子的X原子与原子核外N层上有2个电子的Y原子 |
| C、2p轨道上有一个未成对电子的X原子与3p轨道上有一个未成对电子的Y原子 |
| D、L 层上只有一个空p轨道的X原子与M层有一个空p轨道的Y原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com