
【题目】在容积为V L的某密闭容器中,a mol CO与2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)![]() CH3OH(g)。CO的转化率与温度、压强的关系如图所示:
CH3OH(g)。CO的转化率与温度、压强的关系如图所示:
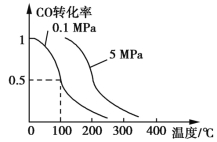
(1)该反应是 反应(填“放热”或“吸热”)。
(2)在压强为0.1 MPa条件下,200 ℃时,该反应的平衡常数K (填“=”“<”或“>”)V2/a2。
(3)在温度、容积不变的情况下,向该密闭容器再增加a mol CO(g)、2a mol H2(g)和b mol CH3OH(g),则达到新平衡时,CO的转化率 (填“增大”“减小”“不变”或“无法确定”),平衡常数 (填“增大”“减小”或“不变”)。
【答案】(1)放热 (2)< (3)无法确定 不变
【解析】(1)从题给图示可知,温度升高,CO的转化率下降,说明升温促使平衡逆向移动,正反应为放热反应。(2)在0.1 MPa压强下,100 ℃时,平衡时各物质的浓度依次为c(CO)=![]() mol·L-1=c(CH3OH),c(H2)=2c(CO)=
mol·L-1=c(CH3OH),c(H2)=2c(CO)=![]() mol·L-1,可逆反应CO(g)+2H2(g)
mol·L-1,可逆反应CO(g)+2H2(g)![]() CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=![]() =
= =
=![]() 。升高温度至200 ℃,平衡左移,K减小,故200 ℃时K<
。升高温度至200 ℃,平衡左移,K减小,故200 ℃时K<![]() 。(3)再加入a mol CO、2a mol H2和b mol CH3OH(g),无法确定平衡的移动,α(CO)无法确定,但温度不变,K不变。
。(3)再加入a mol CO、2a mol H2和b mol CH3OH(g),无法确定平衡的移动,α(CO)无法确定,但温度不变,K不变。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】室温条件下,下列有关电解质溶液的描述正确的是( )
A.向Na2CO3溶液中通入CO2至溶液为中性,则 ![]() >1
>1
B.pH相同的氨水和Ba (OH)2溶液中:2c (NH4+)=c ( Ba2+)
C.等浓度的KHSO3溶液与KOH溶液等体积混合:c(OH﹣)﹣c(H+)=c(HSO3﹣)+c(H2SO3)
D.向Mg (OH)2浊液中加入少量NH4Cl粉末 ![]() 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将固体NH4I置于密闭容器中,在一定温度下发生下列反应:①NH4I(s)![]() NH3(g)+HI(g);②2HI(g)
NH3(g)+HI(g);②2HI(g)![]() H2(g)+I2(g)。达到平衡时,c(H2)=0.5 mol/L,c(HI)=3 mol/L,则此温度下反应①的平衡常数为
H2(g)+I2(g)。达到平衡时,c(H2)=0.5 mol/L,c(HI)=3 mol/L,则此温度下反应①的平衡常数为
A.9 B.16 C.12 D.25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应aA(g)+bB(g)![]() cC(g)+dD(g),达到平衡时,各物质的物质的量浓度应满足以下关系:
cC(g)+dD(g),达到平衡时,各物质的物质的量浓度应满足以下关系:![]() =K,K为一常数,称为化学平衡常数,其反应的K值只与温度有关,现有反应:CO(g)+H2O(g)
=K,K为一常数,称为化学平衡常数,其反应的K值只与温度有关,现有反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0,在850℃时,K=1。
CO2(g)+H2(g) ΔH<0,在850℃时,K=1。
(1)若升高温度到950℃,达到平衡时K________(填“大于”、“小于”或“等于”)1。
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0 mol CO,3.0 mol H2O,1.0 mol CO2和x mol H2,则:
①当x=5.0时,上述平衡向________(填“正反应”或“逆反应”)方向移动。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷是氮族元素,黄砷(As4)是其一种单质,其分子结构与白磷(P4)相似,以下关于黄砷与白磷的比较叙述正确的是
A.分子中共价键键角均为60°B.黄砷中共价键键能大于白磷
C.分子中含有的共价键的数目都是4D.黄砷的熔点低于白磷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示.据图判断正确的是( ) 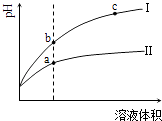
A.Ⅱ为盐酸稀释时的pH值变化曲线
B.b点溶液的导电性比c点溶液的导电性强
C.a点Kw的数值比c点Kw的数值大
D.b点酸的总浓度大于a点酸的总浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极). 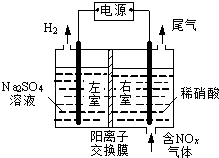
(1)若用NO2气体进行模拟电解法吸收实验. ①写出电解时NO2发生反应的电极反应式: .
②若有标准状况下2.24LNO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为mol.
(2)某小组在右室装有10L0.2molL﹣1硝酸,用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验. ①实验前,配制10L0.2molL﹣1硝酸溶液需量取mL的密度为1.4gmL﹣1、质量分数为63%的浓硝酸.
(3)②电解过程中,有部分NO转化为HNO2 , 实验结束时,测得右室溶液中含3molHNO3、0.1molHNO2 , 同时左室收集到标准状况下28LH2 . 计算原气体中NO和NO2的体积比(假设尾气中不含氮氧化物,写出计算过程).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝基苯是重要的精细化工原料,是医药和染料的中间体,还可做有机溶剂.制备硝基苯的过程如下: ①配制混酸:组装如图反应装置.取100 mL烧杯,用20 mL浓硫酸与浓硝酸18 mL配制混和酸,加入漏斗中.把18 mL苯加入三颈烧瓶中.
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀.
③在50﹣60℃下发生反应,直至反应结束.
④除去混和酸后,粗产品依次用蒸馏水和10%Na2CO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品.已知
(i) ![]() +HNO3(浓)
+HNO3(浓) ![]()
![]() +H2O
+H2O 
(ii)可能用到的有关数据列表如下
物质 | 熔点/℃ | 沸点/℃ | 密度(20℃)/gcm﹣3 | 溶解性 |
苯 | 5.5 | 80 | 0.88 | 微溶于水 |
硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
1,3﹣二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
浓硝酸 | 83 | 1.4 | 易溶于水 | |
浓硫酸 | 338 | 1.84 | 易溶于水 |

请回答下列问题:
(1)配置混酸应先在烧杯中先加入 .
(2)恒压滴液漏斗的优点是 .
(3)实验装置中长玻璃管可用代替(填仪器名称).
(4)反应结束后产品在液体的层(填“上”或者“下”),分离混酸和产品的操作方法为
(5)用10%Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净? .
(6)为了得到更纯净的硝基苯,还须先向液体中加入除去水,然后蒸馏,最终得到17.5g硝基苯,则硝基苯的产率为(保留两位有效数字).若加热后,发现未加沸石,应采取的操作是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com