
| A. | NA个氧气分子与NA个氖气分子的质量比是4:5 | |
| B. | 17gOH-与19gH3O+所含电子数相等 | |
| C. | 32gSO2和40gSO3所含的原子数相等 | |
| D. | 标准状况下,11.2LCO2与常温常压下17gNH3所含分子数相等 |
分析 A.稀有气体为单原子分子,NA个氧气分子与NA个氖气分子的物质的量都是1mol,质量之比为32g:20g=8:5;
B.氢氧根离子、水和氢离子都含有10个电子;
C.质量转化为物质的量,结合1个二氧化硫含有3个原子,1个三氧化硫含有3个原子解答;
D.标况下,11.2L二氧化碳的物质的量为0.5mol,17g氨气的物质的量为1mol.
解答 解:A.NA个氧气分子与NA个氖气分子的物质的量都是1mol,二者质量之比为32g:20g=8:5,故A错误;
B.17g OH-的物质的量为1mol,含有10mol电子,19g H3O+的物质的量为1mol,也含有10mol电子,二者含有的电子数相等,故B正确;
C.32gSO2物质的量为$\frac{32g}{32g/mol}$=1mol,含有3mol原子,40gSO3物质的量为$\frac{40g}{80g/mol}$=0.5mol,含有原子个数为0.5mol×4=2mol,所以二者含的原子数不相等,故C错误;
D.标况下,11.2L二氧化碳的物质的量为0.5mol,17g氨气的物质的量为1mol,二者含的分子数不同,故D错误;
故选:B.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,侧重考查学生对基础知识的灵活运用,题目难度不大.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:推断题
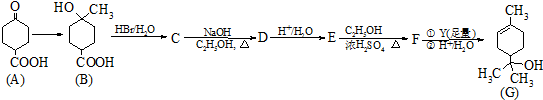
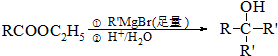
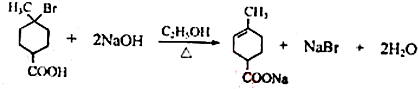 .
.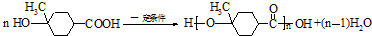 .
.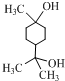 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在碱金属元素中,所有碱金属的氧化物均属于碱性氧化物 | |
| B. | 由于活泼性Na<K,故金属钾可以从NaCl 溶液中置换出钠单质 | |
| C. | 金属锂不能保存在煤油中,金属钾可以保存在煤油中 | |
| D. | 碱金属在自然界中都以游离态存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 所有物质之间均存在化学键 | |
| C. | 由非金属元素可以组成离子化合物 | |
| D. | 不同元素组成的多原子分子里的化学键一定为极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题


 .
. ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
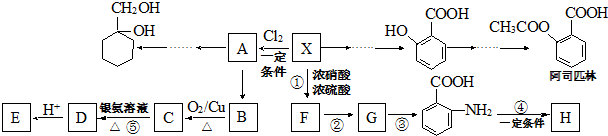
 (苯胺,易被氧化)
(苯胺,易被氧化)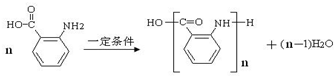 .
.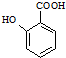 的同系物M比其本身相对分子质量大14,M的同分异构体中能同时满足以下条件:①芳香族化合物,②能发生水解反应,③与FeCl3溶液能够发生显色反应;共有19(不考虑立体异构)种.
的同系物M比其本身相对分子质量大14,M的同分异构体中能同时满足以下条件:①芳香族化合物,②能发生水解反应,③与FeCl3溶液能够发生显色反应;共有19(不考虑立体异构)种.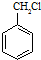 和其他无机物合成
和其他无机物合成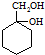 最合理的方案.
最合理的方案.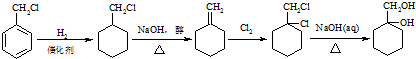 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
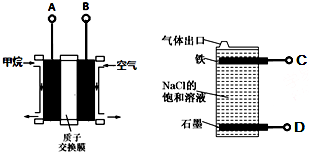
| A. | 燃料电池的A极连接电解池的C极 | |
| B. | 燃料电池工作时当0.2 NA个H+通过质子交换膜移向右边,饱和食盐水中可产生2.24L气体 | |
| C. | A电极的电极反应式为:CH4-8e-+2H2O═CO2+8H+ | |
| D. | 电解池总反应式为NaCl+H2O$\frac{\underline{\;电解\;}}{\;}$NaClO+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com