
| A. | 分子式为C 4H 8的同分异构体共有(不考虑立体异构)5种 | |
| B. | 立方烷(C 8H 8)的六氯取代物有3种 | |
| C. | 分子式为C 5H 10O 2的同分异构体中属于酯的有8种 | |
| D. |  的一溴取代物有4种 的一溴取代物有4种 |
分析 A.分子式为C4H8的同分异构体,可能是烯烃,也可能是环烷烃;
B.六氯取代物的种类等于二氯代物的种类;
C.分子式为C5H10O2的酯为饱和一元酯,形成酯的羧酸与醇的碳原子总数为5,讨论羧酸与醇含有的碳原子,进行书写判断;
D.根据一溴取代物的种类等于有机物中氢原子的种类.
解答 解:A.分子式为C4H8的同分异构体,可能是烯烃:CH2═CH-CH2CH3、CH3CH=CHCH3、CH2=C(CH3)2,也可能是环烷烃:环丁烷、甲基环丙烷,共有5种,故A正确;
B.氯原子可以占据同一边上的两个顶点,同一平面对角线的两个顶点,立方体对角线的两个顶点,故立方烷的二氯代物有3种,而六氯取代物的种类等于二氯代物的种类为3种,故B正确;
C.若为甲酸和丁醇酯化,丁醇有4种,形成的酯有4种:HCOOCH2CH2CH2CH3、HCOOCH2CH(CH3)2、HCOOCH(CH3)CH2CH3、HCOOC(CH3)3;
若为乙酸和丙醇酯化,丙醇有2种,形成的酯有2个:CH3COOCH2CH2CH3、CH3COOCH(CH3)2;
若为丙酸和乙醇酯化,丙酸有1种,形成的酯有1个:CH3CH2COOCH2CH3;
若为丁酸和甲醇酯化,丁酸有2中,形成的酯有2个:CH3CH2CH2COOCH3、(CH3)2CHCOOCH3,分子式为C5H10O2的同分异构体中属于酯的有9种,故C错误;
D. 中含有4种氢原子,所以一溴取代物的种类是4种,故D正确;
中含有4种氢原子,所以一溴取代物的种类是4种,故D正确;
故选C.
点评 本题主要考查同分异构体的判断,题目难度不大,掌握同分异构体的分类和书写方法是解题的关键,试题有利于提高学生的分析能力及综合应用能力.


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:选择题
| A. | 固体硫酸钡不能导电,所以硫酸钡是非电解质 | |
| B. | Cl2的水溶液能导电,所以Cl2是电解质 | |
| C. | NaOH溶液能导电,所以NaOH溶液是电解质 | |
| D. | CO2、SO2、SO3、NH3等均属于非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 利用CO和H2在催化剂的作用下合成甲醇,反应如下:CO(g)+2H2(g)?CH3OH(g).在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示.下列说法正确的是( )
利用CO和H2在催化剂的作用下合成甲醇,反应如下:CO(g)+2H2(g)?CH3OH(g).在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示.下列说法正确的是( )| A. | 该反应的△H<0,且p1<p2<p3 | |
| B. | 在C点时,H2转化率为75% | |
| C. | 反应速率:ν逆(状态A)>ν逆(状态B) | |
| D. | 在恒温恒压条件下,向该密闭容器中再充入1molCH3OH,达平衡时CH3OH的体积分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,向20mL的某稀盐酸中滴入0.1mol•L-1的氨水,溶液中由水电离出的氢离子浓度随滴人氨水体积的变化如图.下列分析不正确的是( )
常温下,向20mL的某稀盐酸中滴入0.1mol•L-1的氨水,溶液中由水电离出的氢离子浓度随滴人氨水体积的变化如图.下列分析不正确的是( )| A. | V2=20 mL | B. | d点溶液中:c(NH4+)>c(Cl-) | ||
| C. | b点溶液中:c(H+)=c(OH-) | D. | 该稀盐酸的浓度为0.1 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,基态f原子的核外电子排布式为1s22s22p63s23p63d104s1.
,基态f原子的核外电子排布式为1s22s22p63s23p63d104s1.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 肯定不存在的离子是Mg2+、Cu2+、SO42-、CO32-,是否含NH4+另需实验验证 | |
| B. | 无法确定原溶液中是否存在Cl- | |
| C. | 肯定存在的离子是SO32-、Br-,是否存在Na+、K+需要通过焰色反应来确定 | |
| D. | 若步骤中Ba(NO3)2和HNO3溶液改用BaCl2和盐酸的混合溶液,则对溶液中离子的判断无影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
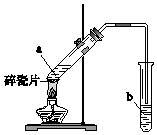 实验室用如图所示装置制备乙酸乙酯.
实验室用如图所示装置制备乙酸乙酯. 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | CH4 | C2H2 | H2 |
| 燃烧热/(kJ/mol) | 890.3 | 1299.6 | 285.8 |
| A. | 2H2(g)+O2(g)═2H2O(g)△H=-571.6kJ/mol | |
| B. | CH4和C2H2中所含化学键完全相同 | |
| C. | 2CH4(g)═C2H2(g)+3H2(g)△H=-376.4kJ/mol | |
| D. | C≡C键能为796.0kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①浊液中存在平衡:Ag2CrO4(s)?2Ag+(aq)+CrO42-(aq) | |
| B. | ②中溶液变澄淸原因:AgOH+2NH3•H2O═[Ag(NH3)2]OH+2H2O | |
| C. | ③中顔色变化说明有AgCl生成 | |
| D. | 该实验可以证明AgCl比Ag2CrO4更难溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com