
| A. | 40 mL | B. | 72 mL | C. | 128 mL | D. | 20 mL |
分析 根据电荷守恒计算出混合溶液中溶液中n(Al3+).由MgCl2和AlCl3的混合溶液与氢氧化钠溶液的反应可知,要使Mg2+全部转化为沉淀分离出来,Al3+应恰好转化为AlO2-,反应后溶液为NaCl、NaAlO2的混合液,根据Na、Cl、Al原子守恒,有n(NaOH)=n(Cl)+n(Al),再根据V=$\frac{n}{c}$计算即可.
解答 解:溶液中n(Cl-)=0.1×0.65mol/L=0.065mol,
溶液中n(Mg2+)=0.1mol/L×0.1L=0.01mol,
所以溶液中n(Al3+)=$\frac{0.065mol-0.01mol×2}{3}$=0.015mol,
将100mL此溶液中的Mg2+转化为Mg(OH)2沉淀并分离析出,反应后溶液为NaCl、NaAlO2的混合液,
由原子守恒可知n(NaOH)=n(Na)=n(Cl)+n(Al)=0.065mol+0.015mol=0.08mol,
所以至少需要2mol/L氢氧化钠溶液的体积为$\frac{0.08mol}{2mol/L}$=0.04L=40ml,
故选A.
点评 本题考查混合物的有关计算,利用原子守恒,简化解题,关键在于清楚反应后溶液为NaCl、NaAlO2的混合液.


科目:高中化学 来源: 题型:选择题
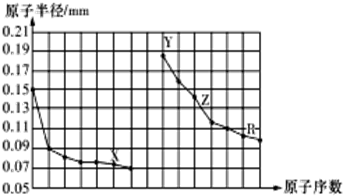
| A. | 同周期元素中,X氢化物的沸点最高 | |
| B. | 简单离子半径:X>Y>Z | |
| C. | Y、Z、R对应的最高价氧化物的水化物相互之间可以发生反应 | |
| D. | 电解熔融的X与Z构成的化合物可以得到单质Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铅蓄电池充电时,阳极的反应为:PbSO4+2H2O+2e-═PbO2+SO42-+4H+ | |
| B. | FeCl2溶液与K3[Fe(CN)6]溶液混合后得到特征蓝色沉淀,利用此反应可检验Fe2+ | |
| C. | 常温下将5mL 0.1 mol/LNa2S2O3溶液、5mL 0.01 mol/LNa2S2O3溶液分别与5mL 0.1 mol/LH2SO4溶液混合并搅拌,通过记录溶液中出现浑浊的时间,可确定浓度对化学反应速率的影响 | |
| D. | 处理含有Hg2+离子的废水可加入硫化钠,使Hg2+离子转化为HgS沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在无色溶液中:K+、Cu2+、SO42-、NO3- | |
| B. | 在含Fe3+的溶液中:NH4+、Na+、Cl、OH- | |
| C. | 在强碱溶液中:Na+、K+、Cl-、CO32- | |
| D. | 在强酸性的溶液中:K+、Na+、Cl-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ①②③ | C. | ③④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最外层有1个电子的原子都是碱金属 | |
| B. | 最外层有5个电子的原子都是非金属原子 | |
| C. | 稀有气体原子最外层都达到8电子稳定结构 | |
| D. | 过渡元素原子的最外层都不超过2个电子,都是金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生活中,用饱和碳酸钠溶液洗去锅碗瓢盆上的油污,且热溶液的效果更好 | |
| B. | 常温下,铁、铝在浓硝酸中钝化 | |
| C. | 侯氏制碱工业中,降温析出副产品NH4Cl之前,向溶液中既撒NaCl固体又通入足量NH3 | |
| D. | 夏天,打开冰镇汽水瓶,立即冒出大量泡沫 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com