
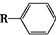
 $”ś_{Ņ»¶ØĢõ¼ž}^{CO£¬HCl}$
$”ś_{Ņ»¶ØĢõ¼ž}^{CO£¬HCl}$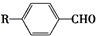 £¬ĪŖŗĻ³ÉijÖÖŅŗ¾§²ÄĮĻµÄÖŠ¼äĢåM£¬ÓŠČĖĢį³öČēĻĀ²»Ķ¬µÄŗĻ³ÉĶ¾¾¶£ŗ
£¬ĪŖŗĻ³ÉijÖÖŅŗ¾§²ÄĮĻµÄÖŠ¼äĢåM£¬ÓŠČĖĢį³öČēĻĀ²»Ķ¬µÄŗĻ³ÉĶ¾¾¶£ŗ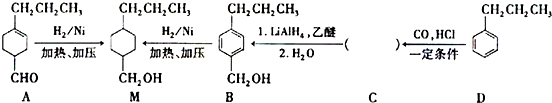
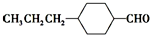 ŗĶ
ŗĶ £ØŠ“½į¹¹¼ņŹ½£©Éś³É£®
£ØŠ“½į¹¹¼ņŹ½£©Éś³É£®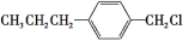 £®
£® ·ÖĪö ÓÉŗĻ³ÉĮ÷³ĢæÉÖŖ£¬A”śM·¢Éś-CHOŗĶC=CµÄ¼Ó³É·“Ó¦£¬B”śMĪŖ±½»·µÄ¼Ó³É·“Ó¦£¬½įŗĻŠÅĻ¢æÉÖŖ£¬D”śC·¢ÉśČ”“ś·“Ó¦£¬ŌņCµÄ½į¹¹¼ņŹ½ĪŖ£ŗCH3CH2CH2C6H4CHO£¬Ćū³ĘĪŖ¶Ō±ū»ł±½¼×Č©£»C”śBµÄ·“Ó¦ĪŖ-CHOµÄ¼Ó³É·“Ó¦£¬Č»ŗó½įŗĻÓŠ»śĪļµÄ½į¹¹ÓėŠŌÖŹ½ųŠŠ½ā“š£®
½ā“š ½ā£ŗÓÉŗĻ³ÉĮ÷³ĢæÉÖŖ£¬A”śM·¢Éś-CHOŗĶC=CµÄ¼Ó³É·“Ó¦£¬B”śMĪŖ±½»·µÄ¼Ó³É·“Ó¦£¬½įŗĻŠÅĻ¢æÉÖŖ£¬D”śC·¢ÉśČ”“ś·“Ó¦£¬CĪŖCH3CH2CH2C6H4CHO£¬Ćū³ĘĪŖ¶Ō±ū»ł±½¼×Č©£¬C”śBĪŖ-CHOµÄ¼Ó³É·“Ó¦£¬
£Ø1£©AĪŖ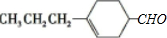 £¬Ęä·Ö×ÓÖŠŗ¬ÓŠ10øöC”¢16øöHŗĶ1øöOŌ×Ó£¬Ęä·Ö×ÓŹ½ĪŖ£ŗC10H16O£»1molAÄܹ»ĻūŗÄŃõĘųµÄĪļÖŹµÄĮæĪŖ£ŗ£Ø10+$\frac{16}{4}$-$\frac{1}{2}$£©mol=13.5mol£¬
£¬Ęä·Ö×ÓÖŠŗ¬ÓŠ10øöC”¢16øöHŗĶ1øöOŌ×Ó£¬Ęä·Ö×ÓŹ½ĪŖ£ŗC10H16O£»1molAÄܹ»ĻūŗÄŃõĘųµÄĪļÖŹµÄĮæĪŖ£ŗ£Ø10+$\frac{16}{4}$-$\frac{1}{2}$£©mol=13.5mol£¬
¹Ź“š°øĪŖ£ŗC10H16O£»13.5£»
£Ø2£©A·Ö×ÓÖŠŗ¬C=C£¬ÄÜÓėäåĖ®·¢Éś¼Ó³É·“Ó¦£¬ĒŅC=C”¢-CHO¾łÄܱ»ĖįŠŌøßĆĢĖį¼ŲŃõ»Æ£¬¶ų±½”¢ŅŅĖįŅŅõ„²»ÓėA·“Ó¦£¬ĖłŅŌÄܹ»ÓėA·“Ó¦µÄĪŖBD£¬
¹Ź“š°øĪŖ£ŗBD£»
£Ø3£©C”śBµÄ·“Ó¦¹ż³ĢĪŖ-CHOµÄ¼Ó³É·“Ó¦£¬Ņ²ŹōÓŚ»¹Ō·“Ó¦£¬
¹Ź“š°øĪŖ£ŗ¼Ó³É·“Ó¦£Ø»ņ»¹Ō·“Ó¦£©£»
£Ø4£©ÓÉA“߻ƼÓĒāÉś³ÉMµÄ¹ż³ĢÖŠ£¬C=C”¢-CHO¾łÄÜÓėĒāĘų·¢Éś¼Ó³É·“Ó¦£¬ŌņÉś³ÉÖŠ¼äĢåĪŖ£ŗ »ņ
»ņ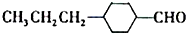 £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø5£©CĪŖCH3CH2CH2C6H4CHO£¬¼ģŃéBÖŠŹĒ·ńŗ¬ÓŠC£¬æĘĄūÓĆČ©»łµÄŠŌÖŹŃ”Ņų°±ČÜŅŗ£Ø»ņŠĀÖĘĒāŃõ»ÆĶŠü×ĒŅŗ£©²śÉśŅų¾µ£Ø»ņשŗģÉ«³Įµķ£©¼“æÉÖ¤Ć÷£¬
¹Ź“š°øĪŖ£ŗŅų°±ČÜŅŗ£Ø»ņŠĀÖĘĒāŃõ»ÆĶŠü×ĒŅŗ£©£»
£Ø6£©BŅ²æÉÓÉC10H13ClÓėNaOHĖ®ČÜŅŗ¹²ČČÉś³É£¬Ģ¼Į“¹Ē¼Ü²»±ä£¬ŌņC10H13ClµÄ½į¹¹¼ņŹ½ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ £®
£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śŗĻ³É£¬ĢāÄæÄѶČÖŠµČ£¬ŹģĮ·ÕĘĪÕ³£¼ūÓŠ»śĪļ½į¹¹ÓėŠŌÖŹĪŖ½ā“š¹Ų¼ü£¬×¢ŅāĆ÷Č·ÓŠ»ś·“Ó¦øÅÄī¼°·“Ó¦ĄąŠĶµÄÅŠ¶Ļ·½·Ø£¬ŹŌĢā²ąÖŲæ¼²éѧɜµÄ·ÖĪö”¢Ąķ½āÄÜĮ¦¼°Āß¼ĶĘĄķÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £®
£®
 £¬
£¬ £¬
£¬ £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
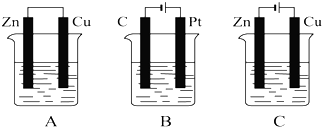
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | C£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH4Cl£Øs£©=NH3£Øg£©+HCl£Øg£©ŹŅĪĀĻĀ²»ÄÜ×Ō·¢½ųŠŠ£¬ĖµĆ÷øĆ·“Ó¦µÄ”÷H£¼0 | |
| B£® | ¶ĘĪżĢśÖĘĘ·¶Ę²ćĘĘĖšŗó£¬ĢśÖĘĘ·±ČŹÜĖšĒ°øüČŻŅ×ÉśŠā£¬¶ų¶ĘŠæĢśÖĘĘ·ŌņĻą·“ | |
| C£® | ½«“æĖ®¼ÓČČÖĮ½ĻøßĪĀ¶Č£¬K±ä“ó”¢pH±äŠ””¢³ŹĖįŠŌ | |
| D£® | øų0.1mol•L-1CH3COOHČÜŅŗÖŠ¼ÓČČ£¬Ōņc£ØH+£©Óėc£ØCH3COOH£©µÄ±ČÖµŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 µÄĻµĶ³ĆüĆū£ŗ3£¬4-¶ž¼×»łŅŃĶé
µÄĻµĶ³ĆüĆū£ŗ3£¬4-¶ž¼×»łŅŃĶé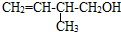 µÄ¼üĻߏ½£ŗ
µÄ¼üĻߏ½£ŗ
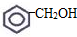 ¢Ū
¢Ū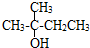 ¢Ü
¢Ü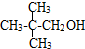 ¢Ż
¢Ż ¢Ž
¢Ž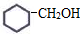
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaOH | B£® | AlCl3 | C£® | K2S | D£® | Cl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
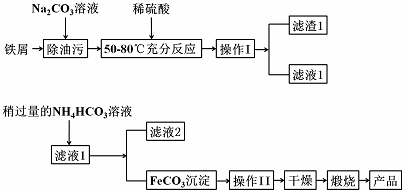
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ūĻ©·Ö×ÓÓŠ8øö¦Ņ¼ü£¬1øö¦Š¼ü | |
| B£® | ±ūĻ©·Ö×ÓÖŠ3øöĢ¼Ō×Ó¶¼ŹĒsp3ŌÓ»Æ | |
| C£® | ±ūĻ©·Ö×ÓÖŠÖ»“ęŌŚ¼«ŠŌ¼ü | |
| D£® | ±ūĻ©·Ö×ÓÖŠ3øöĢ¼Ō×ÓŌŚĶ¬Ņ»Ö±ĻßÉĻ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com