
A、用惰性电极电解饱和MgCl2溶液:2Cl-+2H2O
| ||||
| B、NaHSO4溶液与Ba(OH)2溶液混合后溶液呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | ||||
| C、将标准状况下112 mL氯气通入10 mL 1 mol?L-1的溴化亚铁溶液中:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 | ||||
| D、向澄清石灰水中加入过量的碳酸氢钠溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| ||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、某吸热反应能自发进行,则该反应的△S>0 |
| B、SO2使酸性KMnO4溶液褪色,因此SO2具有漂白性 |
| C、在物质分离的方法中,蒸馏、萃取、重结晶都与物质的溶解度有关 |
| D、用浓硫酸代替稀硫酸与铁反应能加快生成H2的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
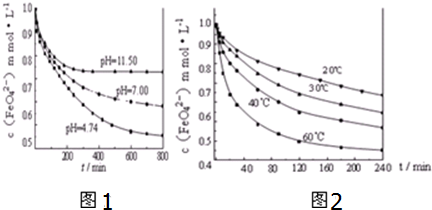
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 化学反应及离子方程式 | 评价 |
| A | 醋酸钠溶于水:CH3COO?+H2O=CH3COOH+OH- | 正确 |
| B | 在氢氧化钠溶液中滴加少量氯化铝: Al3++3OH-=Al(OH)3↓ | 错误,Al(OH)3能溶于氢氧化钠 |
| C | 铁加入到过量的稀硝酸溶液中: 3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O | 正确 |
| D | 在硫酸铝钾溶液中滴加氢氧化钡至沉淀物质的量最多: 3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓ | 错误,Al3+与OH-的化学计量数之比应为1:3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤⑦ | B、②④⑤ |
| C、①③④ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、熵增加且吸热的反应一定是自发反应 |
| B、熵增加且放热的反应一定是自发反应 |
| C、熵减少且放热的反应一定是自发反应 |
| D、熵减少且吸热的反应一定是自发反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 氢氧化钡 | 蔗糖溶液 | 硫酸钡 | 醋酸 | 氢气 |
| B | 胆矾 | 水煤气 | 硫酸 | 醋酸 | 干冰 |
| C | 盐酸 | 石灰水 | 苛性钾 | 水 | 氨气 |
| D | 石灰石 | 水玻璃 | 氯化钙 | 氢氧化铁 | 碳酸钙 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com