
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:问答题
| 温度(K) CO2转化率% n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
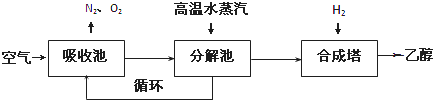
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.高温、高压 |
| B.适宜的温度、高压、催化剂 |
| C.低温、高压、催化剂 |
| D.高温、高压、催化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.增大压强,有利于SO2和O2反应生成SO3 |
| B.热的纯碱溶液去油污能力较强 |
| C.加催化剂使N2和H2在一定条件下转化为NH3 |
| D.常温下,pH=3的H2SO4溶液中水的电离程度小于pH=3的NH4Cl溶液中水的电离程度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.降低温度和增大压强 | B.降低温度和减小压强 |
| C.升高温度和减小压强 | D.升高温度和增大压强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| c(A) |
| c(B) |
| c(A) |
| c(B) |
| A.在该温度下,保持容积固定不变,向容器内补充了B气体,则a<b |
| B.若a=b,则容器中一定使用了催化剂 |
| C.若保持温度、压强不变,充入惰性气体,则有a<b |
| D.若其他条件不变,升高温度,则有a<b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 催化剂 |
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
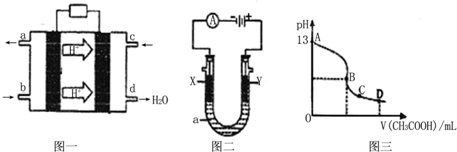
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com