
某1 L混合溶液中,溶质X、Y的浓度都为0.1 mol·L-1,向混合溶液中滴加某溶液Z(0.1 mol· L-1氢氧化钠或硫酸溶液),所得沉淀的物质的量如图所示,则X、Y、Z分别是
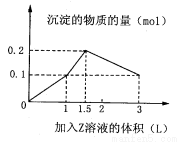
A.硫酸铝、硫酸铁、氢氧化钠
B.硫酸铝、硫酸镁、氢氧化钠
C.偏铝酸钠、氢氧化钡、硫酸
D.偏铝酸钠、氯化钡、硫酸
科目:高中化学 来源:2014-2015甘肃省高一上学期期末考试化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.Fe(OH)3溶于氢碘酸:Fe(OH)3+ 3H+=Fe3++ 3H2O
B.用醋酸除去水垢:CaCO3+2H+=Ca2++ H2O+CO2↑
C.氯气与水的反应:Cl2+H2O=2H++Cl—+ClO—
D.等体积、等浓度的Ca(HCO3)2溶液和NaOH溶液混合:Ca2++HCO3—+OH—=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省白银市高二上学期期末化学试卷(解析版) 题型:填空题
(12分)(1)物质的量浓度相同的三种盐NX、NaY、NaZ的溶液,其pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是 。
(2)比较下列溶液的pH(填“>”“<”或“=”):
①0.1 mol·L-1Na2CO3溶液 0.1 mol·L-1NaHCO3溶液
②0.1 mol·L-1NH4Cl溶液 0.01 mol·L-1NH4C1溶液
(3)把a、b、c、d四块金属片浸泡在稀H2SO4中,用导线两两相连,可以组成各种原电池。若a、b相连,a为负极;c、d相连,c极发生氧化反应;a、c相连,c为正极;b、c相连,电流由c极流向b极,则这四种金属的活动性由强到弱的顺序为 。
(4)将AlCl3溶液蒸干、灼烧,最后所得的固体的主要成份是 。
(5)氯化铁溶液呈 性(填“酸”、“碱”或“中”),原因是(用离子方程式表示):
(6)向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-刚好沉淀完全时,溶液的pH 7(填“>”“<”或“=”),离子反应总方程式为: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省白银市高二上学期期末化学试卷(解析版) 题型:选择题
下列物质中,属于弱电解质的是
A.CO2 B.NH3·H2O C.NH4NO3 D.C2H5OH(酒精)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列实验操作或结论正确的是
A.制备Fe(OH)3胶体时,将饱和的FeCl3溶液滴入沸水中,在加热的同时不断搅拌,直到得到红褐色溶液
B.洗涤沉淀的操作是将沉淀置于滤纸上(已放置在漏斗中),边用玻璃棒搅拌边加蒸馏水冲洗
C.实验室配制950 mL 0.2 mol/L的CuSO4溶液时,需称取胆矾的质量为50 g
D.配液时,液面若超过刻度线,应用胶头滴管将多出液体吸出
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高三上学期第三次月考化学试卷(解析版) 题型:选择题
类比是研究物质性质的常用方法之一,可预测许多物质的性质。但类比是相对的,不能违背客观事实。下列各种类比推测的说法中正确的是
①已知Fe与S能直接化合生成FeS,推测Cu与S可直接化合生成CuS
②已知CaCO3与稀硝酸反应生成CO2,推测CaSO3与稀硝酸反应生成SO2
③已知Br2与Fe反应生成FeBr3,推测I2与Fe生成FeI3
④已知Fe与CuSO4溶液反应,推测Fe与AgNO3溶液也能反应
⑤已知NaOH是强电解质,其饱和溶液导电能力很强,Ca(OH)2也是强电解质,推测其饱和溶液导电能力也很强
A.④ B.①②④⑤ C.③④ D.④⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省天一高三上学期大联考化学试卷(解析版) 题型:填空题
(选考)化学·选修3:物质结构与性质(15分)金属铝、铁、铜与人类生产、生活息息相关。
(1)聚合硫酸铁(简称PFS)的化学式为[Fe(OH)n(SO4)(3—n)/2]m,是常用的水处理剂,与PFS中铁元素价态相同的铁离子的电子排布式为____________。
(2)下列关于[Cu(NH3)4]SO4、K4[Fe(CN)6]、Na3[AlF6]的说法中正确的有_____ (填字母)。
a.三种物质中含有的化学键类型均有离子键和配位键
b.[Cu(NH3)4]SO4中含有NH3分子,其水溶液中也含有大量分子
c.三种物质的组成元素中第一电离能最大的是氮元素
d.K4[Fe(CN)6]与Na3[AlF6]的中心离子具有相同的配位数
(3)氯和钾与不同价态的铜可生成两种化合物,其阴离子均为无限长链结构(如图所示),a位置上的Cl原子的杂化轨道类型为________。已知其中一种化合物的化学式为KCuCl3,则另一种化合物的化学式为________。

(4)用晶体的X射线衍射法可以测得阿伏加德罗常数的值。对金属铜的测定得到以下结果:铜晶胞为面心立方最密堆积,边长为361 pm。又知铜的密度为9 00 g ,则铜原子的直径约为________pm,阿伏加德罗常数的值为_______.
,则铜原子的直径约为________pm,阿伏加德罗常数的值为_______.
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三上学期期末化学试卷(解析版) 题型:实验题
(10分)Na2S2O3·5H2O可作为高效脱氯剂,工业上用硫铁矿(FeS2)为原料制备该物质的流程如下。

已知:I.气体A可以使品红溶液褪色,与硫化氢(H2S)混合能获得单质硫。
II.pH约为11的条件下,单质硫与亚硫酸盐可以共热生成硫代硫酸盐。
回答下列问题:
(1)沸腾炉中将粉碎的硫铁矿用空气吹动使之达到“沸腾”状态,其目的是_____________。
(2)吸收塔中的原料B可以选用____________(填字母序号)。
a.NaCl溶液 b.Na2CO3溶液 c.Na2SO4溶液
(3)某小组同学用下图装置模拟制备Na2S2O3的过程(加热装置已略去)。

①A中使用70%的硫酸比用98%的浓硫酸反应速率快,其原因是______。装置B的作用是_______。
②C中制备Na2S2O3发生的连续反应有:Na2S +H2O +SO2===Na2SO3 +H2S、_____和__________。
(4)工程师设计了从硫铁矿获得单质硫的工艺,将粉碎的硫铁矿用过量的稀盐酸浸取,得到单质硫和硫化氢气体,该反应的化学方程式为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com