
| A. | 1 mol Cl2分别与足量的铁或氢氧化钠溶液反应,转移电子数均为2NA | |
| B. | 1molC5H12分子中共价键总数为14NA | |
| C. | 78gNa2O2固体与足量的H2O反应转移的电子数为NA | |
| D. | 标准状况下,2.24LNH3和CH4的混合气体,所含电子总数为2NA |
分析 A、氯气和铁反应时,完全做氧化剂被还原为-1价;而氯气和氢氧化钠溶液反应时,发生了自身的氧化还原反应;
B、C5H12中含12条C-H键和4条C-C键;
C、求出过氧化钠的物质的量,然后根据过氧化钠和水反应时,1mol过氧化钠转移1mol电子来分析;
D、求出混合物的物质的量,然后根据氨气和甲烷均为10电子分子来分析.
解答 解:A、氯气和铁反应时,完全做氧化剂被还原为-1价,故1mol氯气和铁反应时转移2NA个电子;而氯气和氢氧化钠溶液反应时,发生了自身的氧化还原反应,1mol氯气转移NA个电子,故A错误;
B、C5H12中含12条C-H键和4条C-C键,故1molC5H12中含16NA条共价键,故B错误;
C、78g过氧化钠的物质的量为1mol,而过氧化钠和水反应时,1mol过氧化钠转移1mol电子,故转移NA个电子,故C正确;
D、标况下2.24L氨气和甲烷的混合气体的物质的量为0.1mol,而氨气和甲烷均为10电子分子,故0.1mol混合气体中含NA个电子,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
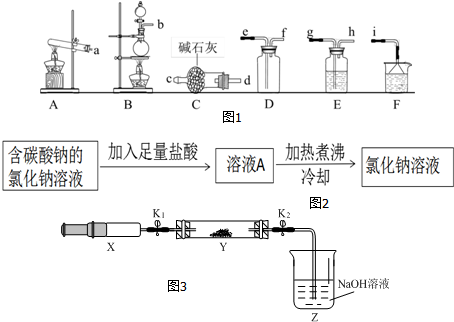
| 实验操作 | 实验现象及结论 |
| 将浸有酚酞溶液的滤纸干燥后,放入盛有干燥氨气的集气瓶中 | 无明显现象 |
| 将浸有酚酞溶液的滤纸湿润后,放入盛有干操氨气的集气瓶中 | 滤纸变红,说明氨气遇水形成溶液呈碱性 |
| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中 | ①Y管中红棕色气体慢慢变浅,最后褪为无色 | ②反应的化学方程式 8NH3+6NO2 $\frac{\underline{\;催化剂\;}}{\;}$7N2+12H2O |
| 将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝聚 |
| 打开K2 | ③Z中的NaOH溶液倒吸入Y管中 | ④该反应是气体体积减小的反应,Y管内压强降低,在大气压的作用下发生倒吸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点HBr>HCl,则同族元素氢化物沸点HCl>HF | |
| B. | Fe3O4可表示为FeO•Fe2O3,则Pb3O4可表示为PbO•Pb2O3 | |
| C. | CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应也只生成Na2SO3和O2 | |
| D. | 因为N元素的非金属性比P元素强,所以HNO3的酸性强于H3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 绿藻的胶质中分离出一种有机化合物(用A表示),结构如图所示,A对人体无害,可用于新鲜食品中对脂肪酶进行抑制来保持风味,也可外用使伤口快速愈合.则关于该物质的说法中错误的有( )
绿藻的胶质中分离出一种有机化合物(用A表示),结构如图所示,A对人体无害,可用于新鲜食品中对脂肪酶进行抑制来保持风味,也可外用使伤口快速愈合.则关于该物质的说法中错误的有( )| A. | 该物质的化学式为C21H26O6 | |
| B. | 该物质中含有两个手性碳原子 | |
| C. | 1 mol 该物质最多能消耗5 mol H2和3 mol NaOH | |
| D. | 该物质能发生加成反应、取代反应、氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应不再进行 | B. | 反应物浓度等于生成物浓度 | ||
| C. | 正反应速率不等于逆反应速率 | D. | 各组分浓度不再随时间而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体粒子能透过滤纸,但不能透过半透膜 | |
| B. | 胶体和溶液的本质区别在于分散质粒子大小 | |
| C. | 蛋清、豆浆、墨水都是胶体 | |
| D. | 丁达尔效应是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4、C2H6 | B. | C2H4、C3H6 | C. | C2H4、C2H4O | D. | C4H8、C6H12O6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com