
 ����Ԫ�ؾ�Ϊ������Ԫ�أ�
����Ԫ�ؾ�Ϊ������Ԫ�أ�| Ԫ�ش��� | �����Ϣ |
| M | �ǽ���Ԫ�أ�����̬�⻯���ˮ��Һ�ʼ��� |
| A | A�ĵ�������ˮ���ҷ�Ӧ���õ�ǿ������Һ |
| B | B��ԭ�������������� �ڲ������������ |
| C | �ڵ��������У�C�ļ����Ӱ뾶��С |
| D | A��B��D��ɵ�36���ӵĻ�����X�Ǽ�������������Ҫ�ɷ� |
| E | �����л����ж�����EԪ�� |
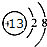 ��
��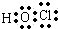 ��
������ ������Ԫ���У��ǽ���Ԫ��M����̬�⻯���ˮ��Һ�ʼ��ԣ���MΪNԪ�أ�A�ĵ�������ˮ���ҷ�Ӧ���õ�ǿ������Һ����AΪNa��B��ԭ�������������� �ڲ��������������ԭ��ֻ����2�����Ӳ㣬����������Ϊ6����BΪOԪ�أ��ڵ��������У�C�ļ����Ӱ뾶��С����CΪAl��A��B��D��ɵ�36���ӵĻ�����X�Ǽ�������������Ҫ�ɷ֣�XΪNaClO��DΪCl�������л����ж�����EԪ�أ���EΪ̼Ԫ�أ�
��� �⣺������Ԫ���У��ǽ���Ԫ��M����̬�⻯���ˮ��Һ�ʼ��ԣ���MΪNԪ�أ�A�ĵ�������ˮ���ҷ�Ӧ���õ�ǿ������Һ����AΪNa��B��ԭ�������������� �ڲ��������������ԭ��ֻ����2�����Ӳ㣬����������Ϊ6����BΪOԪ�أ��ڵ��������У�C�ļ����Ӱ뾶��С����CΪAl��A��B��D��ɵ�36���ӵĻ�����X�Ǽ�������������Ҫ�ɷ֣�XΪNaClO��DΪCl�������л����ж�����EԪ�أ���EΪ̼Ԫ�أ�
��1��BΪOԪ�أ������ڱ��е�λ�ã��ڶ����ڵ� VIA�壬Al3+���ӵĽṹʾ��ͼΪ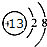 ��
��
�ʴ�Ϊ���ڶ����ڵ� VIA�壻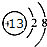 ��
��
��2��D����ͼۺ�����ΪHClO������ʽ Ϊ��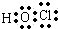 ��
��
�ʴ�Ϊ��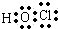 ��
��
��3��M�ļ���̬�⻯��ΪNH3���������γ�ȼ�ϵ�أ�KOHΪ���Һ������������������Ӧ�������ٸ���ʧȥ���ӣ��������������ɵ�����ˮ��������Ӧ����ʽΪ��2NH3-6e-+6OH-�TN2+6H2O��
�ʴ�Ϊ��2NH3-6e-+6OH-�TN2+6H2O��
��4����Cl��C��ɵķ��ӳ���������ṹ�Ļ�����YΪCCl4��Na��CCl4��Ӧ����2�ֹ������ʣ�����һ������Ȼ����Ӳ���������ʣ�������Ϊ���ʯ����Ӧ�������Ȼ��ƣ��÷�Ӧ�Ļ�ѧ����ʽ��4Na+CCl4$\frac{\underline{\;��ո�ѹ\;}}{\;}$4NaCl+C��
�ʴ�Ϊ��4Na+CCl4$\frac{\underline{\;��ո�ѹ\;}}{\;}$4NaCl+C��
��5������Na��O��C��ɵ�һ�������еij����Σ�����A��Na������������Ϊ43%����AΪNa2CO3����ˮ��Һ���������ʵ�����Ϊ1��1��Ӧ�����ӷ���ʽΪ��CO32-+Cl2+H2O=ClO-+Cl-+HCO-3��
�ʴ�Ϊ��CO32-+Cl2+H2O=ClO-+Cl-+HCO-3��
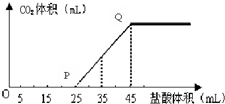
��6����OP��һ��������Ӧ��Na2CO3+HCl=NaHCO3+NaCl��PQ�η�����NaHCO3+HCl�TNaCl+H2O+CO2������OP�����ĵ��������PQ�����ĵ����ᣬ��XΪNaOH��Na2CO3�Ļ���
�ʴ�Ϊ��NaOH��Na2CO3��
OA����������Ӧ��NaOH+HCl=NaCl+H2O��Na2CO3+HCl=NaHCO3+NaCl��
�ڵ�����35mL����ʱ����10mL���ᷴӦ���ɶ�����̼�������ʵ���Ϊ1mol/L��0.01L=0.01mol����NaHCO3+HCl�TNaCl+H2O+CO2������֪���ɶ�����̼Ϊ0.01mol������CO2�����Ϊ0.01mol��22.4L/mol=0.224L����Ϊ22.4mL��
�ʴ�Ϊ��224��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��漰����ʽ��ԭ��ء������ļ���ȣ���Ŀ�Ѷ��еȣ���4���йؼ��Ǹ���ͼ���ж���Һ���ʵijɷ֣�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  Al��OH��3 | B�� |  C6H12O6 | C�� |  CH3CH2OH | D�� |  NaHCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4�� | B�� | 6�� | C�� | 8�� | D�� | 9�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2�� | B�� | 3�� | C�� | 4�� | D�� | 5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
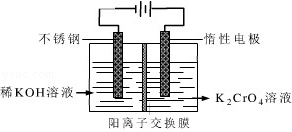 ��������������Ԫ�أ�����֬���л��������ϵ������������������Ⱦ��Σ�����ཡ����
��������������Ԫ�أ�����֬���л��������ϵ������������������Ⱦ��Σ�����ཡ����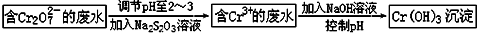
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
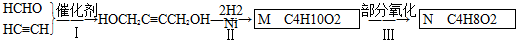
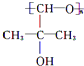

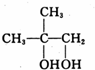 ��B�еĹ�����������ȩ���ʹ��ǻ���
��B�еĹ�����������ȩ���ʹ��ǻ���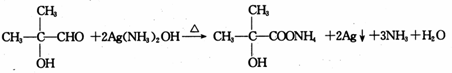 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaCl�к�������Na2SO4�������Ȼ����� | |
| B�� | FeSO4 �к�������CuSO4�����ۣ� | |
| C�� | SO2�к�������HCl���壨����������Һ�� | |
| D�� | CO2�к���������CO�����ȵ�����ͭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com