
分析 依据化学三行计算列式,化学反应速率之比等于化学方程式计量数之比计算得到m,
5min后,测得P的浓度为0.5mol•L-1,Z的平均反应速率是0.1mol/(L•min),v(P)=$\frac{0.5mol/L}{5min}$=0.1mol/L•min,v(Z)=0.1mol/(L•min),则m=2,n(P)=0.5mol/L×2L=1mol,n(Z)=0.1mol/(L•min)×2L×5min=1mol,
3X(g)+Y(g)?2Z(g)+2P(g)
起始量(mol) 2 2 0 0
变化量(mol) 1.5 0.5 1 1
5min量(mol) 0.5 1.5 1 1
(1)上述计算得到m=2;
(2)Y反应速率v=$\frac{△c}{△t}$;
(3)X转化率=$\frac{消耗量}{转化量}$×100%;
(4)气体压强之比等于气体物质的量之比;
解答 解:化学反应速率之比等于化学方程式计量数之比计算得到m,5min后,测得P的浓度为0.5mol•L-1,Z的平均反应速率是0.1mol/(L•min),v(P)=$\frac{0.5mol/L}{5min}$=0.1mol/L•min,v(Z)=0.1mol/(L•min),则m=2,n(P)=0.5mol/L×2L=1mol,n(Z)=0.1mol/(L•min)×2L×5min=1mol,依据化学三行计算列式,
3X(g)+Y(g)?2Z(g)+2P(g)
起始量(mol) 2 2 0 0
变化量(mol) 1.5 0.5 1 1
5min量(mol) 0.5 1.5 1 1
(1)上述计算得到m=2,
答:m的值为2;
(2)Y反应速率v=$\frac{△c}{△t}$=$\frac{\frac{0.5mol}{2L}}{5min}$=0.05mol/L•min,
答:Y的平均反应速率为0.05mol/L•min;
(3)X转化率=$\frac{消耗量}{转化量}$×100%=$\frac{1.5mol}{2mol}$×100%=75%,
答:X的转化率为75%;
(4)气体压强之比等于气体物质的量之比,反应前后气体物质的量不变,气体压强不变,容器中反应开始与5min时的压强比=(2+2):(0.5+1.5+1+1)=1:1,
答:容器中反应开始与5min时的压强比为1:1;
点评 本题考查了化学反应速率概念、化学反应速率计算、气体压强之比等于气体物质的量之比等知识点,主要是三行计算方法和概念实质理解应用,题目较简单.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题


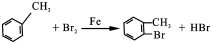 ,F的结构简式
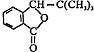
,F的结构简式 .
.
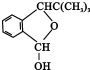 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 |
| $\frac{P}{{P}_{0}}$ | 1.00 | 1.50 | 1.80 | 2.20 | 2.30 | 2.38 | 2.40 | 2.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③④① | C. | ④③②① | D. | ②③①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
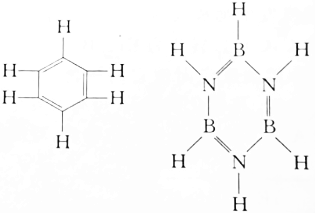
| A. | 前者大于后者 | B. | 前者等于后者 | C. | 前者小于后者 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:| 测定次数 | 待测液体积/mL | 标准盐酸体积/mL | |
| 滴定前读数/mL | 滴定后读数/mL | ||
| 第一次 | 25.00 | 0.40 | 20.38 |
| 第二次 | 25.00 | 4.00 | 24.02 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
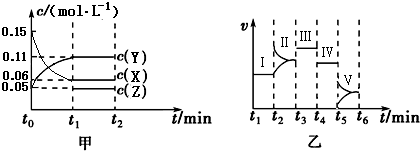
 2Y(g)+Z(g)△H=-10akJ/mol.在乙图Ⅰ~Ⅴ处平衡中,平衡常数最大的是Ⅴ.
2Y(g)+Z(g)△H=-10akJ/mol.在乙图Ⅰ~Ⅴ处平衡中,平衡常数最大的是Ⅴ.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热饱和三氯化铁溶液制备氢氧化铁胶体:Fe3++3H2O$\stackrel{△}{?}$Fe(OH)3(胶体)+3H+ | |
| B. | 硫氢根离子的电离方程式:HS-+H2O?H3O++S2- | |
| C. | 少量氢氧化钙溶液与碳酸氢钠溶液混合的离子方程式:Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- | |
| D. | 0.5mol•L-1的K2Cr2O7溶液中存在如下平衡:Cr2O72-+H2O?2CrO42-+2H+,其平衡常数K的表达式为K=$\frac{{c}^{2}(Cr{{O}_{4}}^{2-})•{c}^{2}({H}^{+})}{c(C{r}_{2}{{O}_{7}}^{2-})}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com