
¹¤ŅµÉĻŅŌCuFeS2ĪŖŌĮĻŅ±Į¶Ķ
 µÄÖ÷ŅŖ·“Ó¦ĪŖ¢Ł2CuFeS2+4O2=Cu2S+3SO2+2FeO (ĀÆŌü£©£»
µÄÖ÷ŅŖ·“Ó¦ĪŖ¢Ł2CuFeS2+4O2=Cu2S+3SO2+2FeO (ĀÆŌü£©£»
¢Ś2Cu2S+3O2= 2Cu2O+2SO2;¢Ū2Cu2O+Cu2S=6Cu+SO2”üĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø £©
2Cu2O+2SO2;¢Ū2Cu2O+Cu2S=6Cu+SO2”üĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø £©
A£®ÓÉ 1 mol CuFeS2 Éś³É 1mol Cu£¬¹²ĻūŗÄ 2.75 molO2
B£®øĆŅ±Į¶·½·ØÖŠ²śÉś“óĮæµÄÓŠŗ¦ĘųĢåSO2,æÉ»ŲŹÕÓĆÓŚÖʱøĮņĖį
C£®ŌŚ·“Ó¦¢ŪÖŠ£¬Cu2S¼ČŹĒŃõ»Æ¼Į£¬ÓÖŹĒ»¹Ō¼Į
D£®ŌŚ·“Ó¦¢ŁÖŠ£¬SO2¼ČŹĒŃõ»Æ²śĪļ£¬ÓÖŹĒ»¹Ō²śĪļ
 53ĖęĢĆ²āĻµĮŠ“š°ø
53ĖęĢĆ²āĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğøŹĖąŹ”øßŅ»ÉĻµŚŅ»“Īѧ¶Īæ¼ŹŌ»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĪŅĆĒµÄÉś»īĄė²»æŖ»Æѧ”£ĻĀĮŠ¶Ō»Æѧɜ»īµÄŠšŹö£¬“ķĪóµÄŹĒ ( )
A. ”°É³ĄļĢŌ½š”±ŹĒĄūÓĆ½šÓėɳµÄĆܶČĻą²ī½Ļ“ó¶ų½«É³ĢŌ×ߏ¹½šĮōĻĀ”£
B. »ÆѧÉĻĖłÖøµÄ ”°ŌÓÖŹ”±£¬ÓŠµÄ±¾Ą“ĪŽŗ¦ĒŅŗÜÓŠ¼ŪÖµ£¬¼“Ź¹ÓŠŗ¦ĪŽ¼ŪÖµµÄŅ²Ó¦Éč·Ø±ä·ĻĪŖ±¦”£
C. ĪŖĮĖĒ×ÉķĢåŃéĪļÖŹµÄŠŌÖŹ£¬ĪŅĆĒÓŠ±ŲŅŖĒ×æŚ³¢Ņ»³¢ĪļÖŹµÄĪ¶µĄ”£
D. ĮĄÉ¹ŅĀ·žŹµ¼ŹÉĻŅ²ŹĒ”°Õō·¢”±”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ½ĖÕŹ”ÄĻĶØŹŠČē¶«ĻŲŠģÖŻŹŠ·įĻŲøßČż10ŌĀĮŖæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ¹ŲŌŖĖŲ¼°Ęä»ÆŗĻĪļµÄ±ķŹ¾ÕżČ·µÄŹĒ
A£®CaH2µÄµē×ÓŹ½£ŗ[H:]‑Ca2+[:H]-
B£®Cl-µÄ½į¹¹Ź¾ŅāĶ¼£ŗ
C£®ÖŹ×ÓŹżĪŖ92”¢ÖŠ×ÓŹżĪŖ146µÄUŌ×Ó£ŗ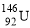
D£®2,4,6-ČżĻõ»ł±½¼×Ėį½į¹¹¼ņŹ½£ŗ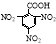
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗž±±Ź”øßČżĮŖŗĻæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠø÷×éĪļÖŹÖŠ£¬³£ĪĀĻĀY¼ČÄÜÓėX·“Ó¦ÓÖÄÜÓėZ·“Ó¦µÄŹĒ
Ń”Ļī | X | Y | Z |
A | SO2 | NaClOČÜŅŗ | CO2 |
B | ŃĪĖį | ÅØĮņĖį | Cu |
C | NH3 | O2 | Mg |
D | Na2O2 | H2O | SiO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”øßČżÉĻµŚŅ»“ĪĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
Ņ»ÖÖŗ¬ĀĮ”¢ļ®”¢īܵĊĀŠĶµē×Ó²ÄĮĻ£¬Éś²śÖŠ²śÉśµÄ·ĻĮĻŹżĮææɹŪ£¬·ĻĮĻÖŠµÄĀĮŅŌ½šŹōĀĮ²µÄŠĪŹ½“ęŌŚ;  īÜŅŌCo2O3 ”¤CoOµÄŠĪŹ½“ęŌŚ£¬Īüø½ŌŚĀĮ²µÄµ„Ćę»ņĖ«Ćę£»ļ®»ģŌÓÓŚĘäÖŠ”£“Ó·ĻĮĻÖŠ»ŲŹÕŃõ»ÆīÜ(CoO)µÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
īÜŅŌCo2O3 ”¤CoOµÄŠĪŹ½“ęŌŚ£¬Īüø½ŌŚĀĮ²µÄµ„Ćę»ņĖ«Ćę£»ļ®»ģŌÓÓŚĘäÖŠ”£“Ó·ĻĮĻÖŠ»ŲŹÕŃõ»ÆīÜ(CoO)µÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
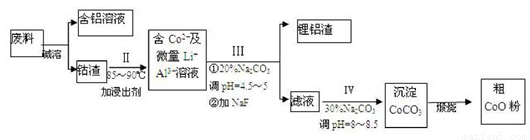
£Ø1£©¹ż³ĢIÖŠ²ÉÓĆNaOHČÜŅŗČܳö·ĻĮĻÖŠµÄAl£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
£Ø2£©¹ż³ĢIIÖŠ¼ÓČėĻ”H2SO4Ėį»Æŗó£¬ŌŁ¼ÓČėNa2S2O3ČÜŅŗ½ž³öīÜ.Ōņ½ž³öīܵĥė×Ó·“Ó¦·½³ĢŹ½ĪŖ£Ø²śĪļÖŠÖ»ÓŠŅ»ÖÖĖįøł£© ”£ŌŚŹµŃéŹŅÄ£Äā¹¤ŅµÉś²śŹ±£¬Ņ²æÉÓĆŃĪĖį“śĢęĖį»ÆµÄNa2S2O3,µ«Źµ¼Ź¹¤ŅµÉś²śÖŠ²»ÓĆŃĪĖį£¬Ēė“Ó·“Ó¦ŌĄķ·ÖĪö²»ÓĆŃĪĖį½ž³öīܵÄÖ÷ŅŖŌŅņ ”£
£Ø3£©ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾¹ż³ĢIIIŗĶIVÖŠNa2CO3µÄÖ÷ŅŖ×÷ÓĆ ”£
£Ø4£©CoOČÜÓŚŃĪĖįæɵƷŪŗģÉ«µÄCoCl2ČÜŅŗ£®CoCl2ŗ¬½į¾§Ė®ŹżÄæ²»Ķ¬¶ų³ŹĻÖ²»Ķ¬ŃÕÉ«£¬ĄūÓĆĄ¶É«µÄĪŽĖ®CoCl2 ĪüĖ®±äÉ«ÕāŅ»ŠŌÖŹæÉÖĘ³É±äÉ«Ė®ÄąŗĶĻŌŅžÄ«Ė®.Ķ¼2ŹĒ·ŪŗģÉ«µÄCoCl2”¤6H2O¾§ĢåŹÜČČ·Ö½āŹ±£¬Ź£Óą¹ĢĢåÖŹĮæĖęĪĀ¶Č±ä»ÆµÄĒśĻߣ¬AĪļÖŹµÄ»ÆѧŹ½ŹĒ £®

£Ø5£©Ä³ĢģČ»¼īµÄ»ÆѧŹ½æɱķŹ¾ĪŖ2Na2CO3”¤NaHCO3”¤2H2O,ȔɣĮæøĆĪļÖŹČÜÓŚĖ®µĆĻ”ČÜŅŗ”£ĻĀĮŠÓŠ¹ŲøĆČÜŅŗÖŠĪ¢Į£µÄĪļÖŹµÄĮæÅØ¶Č¹ŲĻµ ÕżČ·µÄŹĒ £ØĢīŠņŗÅ£©”£
ÕżČ·µÄŹĒ £ØĢīŠņŗÅ£©”£
A£®c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
B£®c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
C£®3c(Na+)>5c(CO32-)+5c(HCO3-)
D£®½«øĆČÜŅŗÓėÉŁĮæNaOH ČÜŅŗ»ģŗĻ£ŗc(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
ČÜŅŗ»ģŗĻ£ŗc(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓÄĻŹ”øßČżÉĻµŚŅ»“ĪĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
°²Č«ŹĒĖ³Ąū½ųŠŠŹµŃé¼°±ÜĆāÉĖŗ¦µÄ±£ÕĻ.ĻĀĮŠŹµŃé²Ł×÷ÕżČ·ĒŅ²»ŹĒ“ÓŹµŃé°²Č«½Ē¶Čæ¼ĀĒµÄŹĒ£Ø £©

A. ²Ł×÷¢Ł£ŗŹ¹ÓĆÉŌ½žČėŅŗĆęĻĀµÄµ¹æŪĀ©¶·¼ģŃéĒāĘųµÄ“æ¶Č
B. ²Ł×÷¢Ś£ŗŹ¹ÓĆCCl4ŻĶČ”äåĖ®ÖŠµÄäåŹ±£¬Õńµ“ŗóŠč“ņæŖ»īČūŹ¹Ā©¶·ÄŚĘųĢå·Å³ö
C. ²Ł×÷¢Ū£ŗĪüŹÕ°±Ęų»ņĀČ»ÆĒāĘųĢå²¢·ĄÖ¹µ¹Īü
D. ²Ł×÷¢Ü£ŗÓĆŹ³Öø¶„×”ĘæČū£¬ĮķŅ»Ö»ŹÖĶŠ×”Ęæµ×£¬°ŃĘæµ¹Į¢£¬¼ģ²éČŻĮæĘæŹĒ·ńĀ©Ė®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 »Æѧ·“Ó¦ĖŁĀŹÓė»ÆŃ§Ę½ŗā
»Æѧ·“Ó¦ĖŁĀŹÓė»ÆŃ§Ę½ŗā| ĪĀ¶Č | 250”ę | 300”ę | 350”ę |
| K | 2.041 | 0.270 | 0.012 |
| ””ŹµŃ鱹ŗÅ | ””T£Ø”ę£© | $\frac{n£ØCO£©}{n£Ø{H}_{2}£©}$ | ””P£ØMPa£© |
| ””i | ””150 | $\frac{1}{3}$ | ””0.1 |
| ””ii | 150 | $\frac{1}{3}$ | 5 |
| ””iii | ””350 | $\frac{1}{3}$ | ””5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | 0.1 mol•L-1CH3COONaČÜŅŗÖŠ£ŗc£ØCH3COO-£©+c£ØCH3COOH£©ØT0.1 mol•L-1 | |
| B£® | 25”ꏱ£¬µČĪļÖŹµÄĮæÅØ¶ČµÄø÷ČÜŅŗpH¹ŲĻµĪŖ£ŗpH£ØNa2CO3£©£¾pH£ØC6H5ONa£©£¾pH£ØNaHCO3£©£¾pH£ØCH3COONa£© | |
| C£® | 25”ꏱ£¬pH=9.4£¬ÅØ¶Č¾łĪŖ0.1 mol•L-1µÄHCNÓėNaCNµÄ»ģŗĻČÜŅŗÖŠ£ŗc£ØNa+£©£¾c£ØHCN£©£¾c£ØCN-£©£¾c£ØOH-£© | |
| D£® | ½«×ćĮæAgCl·Ö±š·ÅČė£ŗ¢Ł5mĖ®£¬¢Ś10mL0.2mol/LMgC12£¬¢Ū20mL0.3mol/LŃĪĖįÖŠČܽāÖĮ±„ŗĶ£¬c£ØAg+£©£ŗ¢Ł£¾¢Ś£¾¢Ū |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com