
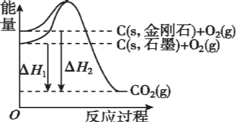
【题目】如图所示,ΔH1=-393.5 kJ·mol-1,ΔH2=-395.4 kJ· mol-1,下列说法或热化学方程式正确的是
A.C(s,石墨)=C(s,金刚石) ΔH=+1.9 kJ· mol-1
B.拆开1mol金刚石和1mol O2中的化学键需要吸收395.4kJ的热量
C.金刚石的稳定性强于石墨
D.石墨的总键能比金刚石的总键能小1.9 kJ
【答案】A
【解析】
先根据图示写出对应的热化学方程式,然后根据盖斯定律写出石墨转变成金刚石的热化学方程式,最后结合物质的能量越低越稳定以及△H=生成物的总能量-反应物的总能量分析解答。
A.由图得:①C(s,石墨)+O2(g)=CO2(g)△H=-393.5kJmol-1,②C(s,金刚石)+O2(g)=CO2(g)△H=-395.4kJmol-1,根据盖斯定律,将①-②可得:C(s,石墨)=C(s,金刚石) △H=+1.9kJmol-1,故A正确;
B.由图得:C(s,金刚石)+O2(g)=CO2(g) △H=-395.4kJmol-1,则拆开1mol金刚石和1mol O2中的化学键需要吸收的能量比形成2molC=O键放出的能量少395.4kJ,故B错误;
C.根据图示,金刚石能量大于石墨的总能量,物质的能量越大,越不稳定,则石墨比金刚石稳定,故C错误;
D.依据热化学方程式 C(s,石墨)=C(s,金刚石) △H=+1.9kJmol-1,所以1mol石墨本身具有的总能量比1mol金刚石本身具有的总能量小1.9 kJ,故D错误;
故选A。


科目:高中化学 来源: 题型:
【题目】下列化学反应的有机产物中有且仅有一种结构的是
A.异戊二烯![]()
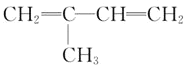
![]() 与等物质的量的
与等物质的量的![]() 发生加成反应
发生加成反应
B.2-氯丁烷(CH3CHClCH2CH3)与NaOH乙醇溶液共热发生消去HCl的反应
C.甲苯在一定条件下发生硝化生成一硝基甲苯的反应
D.邻羟基苯甲酸与NaHCO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语对事实的表述正确的是
A.电解CuCl2溶液:CuCl2=Cu2++2Cl-
B.Mg和Cl形成离子键的过程:![]()
C.向Al2(SO4)3溶液中滴加Na2CO3溶液:2Al3++3CO32-=Al2(CO3)3↓
D.乙酸与乙醇发生酯化反应:CH3COOH+C2H518OH![]() CH3CO18OC2H5+H2O
CH3CO18OC2H5+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别在三个容积均为2.0L的恒容密闭容器中发生反应:A(g)+B(g)D(g)。其中容器甲中反应进行至5min时达到平衡状态,相关实验数据如表所示:
容器 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | 化学平衡常数 | ||
n(A) | n(B) | n(D) | n(D) | |||
甲 | 500 | 4.0 | 4.0 | 0 | 3.2 | K1 |
乙 | 500 | 4.0 | a | 0 | 2.0 | K2 |
丙 | 600 | 2.0 | 2.0 | 2.0 | 2.8 | K3 |
下列说法不正确的是
A.0~5min内,甲容器中A的平均反应速率v(A)=0.64mol·L-1·min-1
B.a=2.2
C.若容器甲中起始投料为2.0molA、2.0molB,反应达到平衡时,A的转化率小于80%
D.K1=K2>K3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面四个反应中,反应类型与其它三个不同的是
A.CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
B.CH3CH2Br+NaOH![]() CH3CH2OH+NaBr
CH3CH2OH+NaBr
C.C6H5OH+3Br2 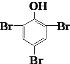 +3HBr
+3HBr
D.2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸可用于合成药物达菲,其结构简式如图( 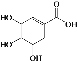 ),下列关于莽草酸的说法正确的是
),下列关于莽草酸的说法正确的是
A.分子式为C7H8O5
B.属于芳香族化合物,含有2种含氧官能团
C.可与碳酸氢钠溶液反应产生无色无味气体
D.可与氢气发生加成反应,1mol莽草酸最多消耗2mol氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氯化氢为原料通过直接氧化法可以制取氯气,反应方程式为:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) 。
(1)该法可按下列催化过程进行:
CuCl2(s)CuCl(s)+![]() Cl2(g) ΔH1=83 kJ·mol-1
Cl2(g) ΔH1=83 kJ·mol-1
CuCl(s)+![]() O2(g)CuO(s)+
O2(g)CuO(s)+![]() Cl2(g) ΔH2=-20 kJ·mol-1
Cl2(g) ΔH2=-20 kJ·mol-1
CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ΔH3=-121 kJ·mol-1
①总反应4HCl(g)+O2(g)2Cl2(g)+2H2O(g)的ΔH=____kJ·mol-1。
②有利于提高总反应平衡产率的条件有______。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(2)恒温恒压下,可以说明总反应4HCl(g)+O2(g)2Cl2(g)+2H2O(g)达到平衡的是_________。
A.压强不变
B.氯气的体积分数保持不变
C.每生成2个H—O的同时,有4个H—Cl生成
D.反应速率v正(O2)∶v逆(H2O)=1∶2
E.各组分的物质的量浓度都相等

(3)密闭容器中充入HCl和O2进行反应,c(HCl)随时间t的变化曲线如图1,保持其他条件不变,t2时升温,t3时重新达平衡,画出t2—t4时c(Cl2)随时间t的变化曲线____。
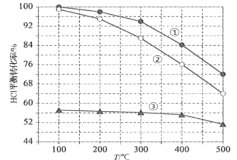
(4)在刚性容器中,进料浓度比c(HCl) ∶c(O2)分别等于1∶1、4∶1、7∶1时,HCl平衡转化率随温度变化的关系如图2:
①其中曲线①代表的c(HCl) ∶c(O2)是__________,原因__________。
②设HCl初始浓度为c0,根据进料浓度比c(HCl)∶c(O2)=4∶1的数据计算K(400℃)=__________(列出计算式,不必算出结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光呼吸是所有进行光合作用的细胞在光照和高氧低二氧化碳情况下发生的一个代谢过程。它是光合作用一个损耗能量的副反应。即绿色植物在照光条件下的呼吸作用。特点是有机物在被分解转化过程中虽也放出CO2,但不能生成ATP,使光合产物被白白地耗费掉。所以光呼吸越强,光合生产率相对就低。
光呼吸现象产生的分子机制是O2和CO2竞争Rubisco酶。在暗反应中,Rubisco酶能够以CO2为底物实现CO2的固定,而当O2浓度高、CO2浓度低时,O2会竞争Rubisco酶。Rubisco酶以O2为底物,对五碳化合物进行加氧氧化。光呼吸使光合作用产物损失的具体过程如图所示。
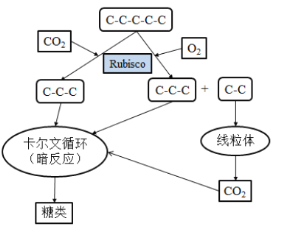
水稻、小麦等C3植物的光呼吸显著,通过光呼吸损耗光合作用新形成有机物的1/4,而高粱、玉米等C4植物的光呼吸消耗很少,只占光合作用新形成有机物的2%~5%。与C3植物相比,C4植物代谢的不同点是,C4植物叶肉细胞的细胞质基质具有一种特殊的PEP羧化酶,它催化如下反应:PEP+HCO3—→苹果酸(C4)+Pi。苹果酸进入维管束鞘细胞,生成CO2用于暗反应,再生出的丙酮酸(C3)回到叶肉细胞中,进行循环利用。叶肉细胞包围在维管束鞘细胞四周,形成花环状结构。PEP羧化酶与CO2的亲和力是Rubisco酶的60倍,也就是PEP羧化酶能固定低浓度的CO2。

水稻和小麦作为养活全世界几乎40%人口的主要作物,它们的产量近几年越来越难满足全球快速增长的食物需求。目前,国际上有很多科研人员致力于提高水稻、小麦的光合速率的研究,旨在提高粮食作物产量。
(1)在光呼吸过程中,有机物被氧化分解,却无ATP生成,而ATP能应用于___________________(写出三条)等生命活动中,故会造成有机物浪费的结果。
(2)有观点指出,光呼吸的生理作用在于高温天气和过强光照下,蒸腾作用过强,植物失水过多,____________大量关闭,导致CO2供应减少。此时的光呼吸可以消耗光反应阶段生成的多余的____________,并且光呼吸的最终产物还可以作为暗反应阶段的原料,这是有重要正面意义的。
(3)综合文中信息,请解释C4植物光呼吸比C3植物小很多的原因__________。
(4)请根据高中所学知识和本文中的信息,在基因水平上写出两条具体的提高水稻、小麦光合作用的研究思路__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CPAE是蜂胶的主要活性成分,也可由咖啡酸合成,下列说法不正确的是( )
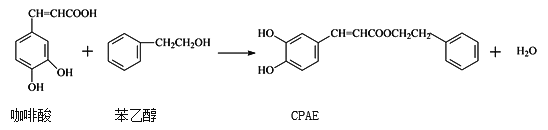
A. 1mol CPAE与足量的溴水反应,最多消耗4mol Br2
B. 咖啡酸可发生聚合反应,而且其分子中含有3种官能团
C. 与苯乙醇互为同分异构体的酚类物质共有9种
D. 可用金属Na检测上述反应是否残留苯乙醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com