
ŅŃÖŖ25 ”ę”¢101 kPaĻĀ£¬ŗ¬1 molĢ¼Ō×ӵďÆÄ«ĶźČ«Č¼ÉÕÉś³ÉCO2·Å³öČČĮæ393.51 kJ£»ŗ¬1 molĢ¼Ō×ӵĽšøÕŹÆĶźČ«Č¼ÉÕÉś³ÉCO2·Å³ö395.41 kJµÄČČĮ攣¾Ż“ĖÅŠ¶Ļ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
| A£®ÓÉŹÆÄ«Öʱø½šøÕŹÆŹĒĪüČČ·“Ó¦£»µČÖŹĮæŹ±£¬ŹÆÄ«µÄÄÜĮæ±Č½šøÕŹÆµÄµĶ |
| B£®ÓÉŹÆÄ«Öʱø½šøÕŹÆŹĒĪüČČ·“Ó¦£»µČÖŹĮæŹ±£¬ŹÆÄ«µÄÄÜĮæ±Č½šøÕŹÆµÄøß |
| C£®ÓÉŹÆÄ«Öʱø½šøÕŹÆŹĒ·ÅČČ·“Ó¦£»µČÖŹĮæŹ±£¬ŹÆÄ«µÄÄÜĮæ±Č½šøÕŹÆµÄµĶ |
| D£®ÓÉŹÆÄ«Öʱø½šøÕŹÆŹĒ·ÅČČ·“Ó¦£»µČÖŹĮæŹ±£¬ŹÆÄ«µÄÄÜĮæ±Č½šøÕŹÆµÄøß |
A
½āĪöŹŌĢā·ÖĪö£ŗÓÉÓŚŌŚĻąĶ¬µÄĶā½ēĢõ¼žĻĀ1 molĢ¼Ō×ӵďÆÄ«Óė½šøÕŹÆ·“Ó¦²śÉśCO2·Å³öČČĮ潚øÕŹÆ±ČŹÆÄ«¶ą£¬ĖµĆ÷µČÖŹĮæŹ±£¬ŹÆÄ«µÄÄÜĮæ±Č½šøÕŹÆµÄµĶ”£ĪļÖŹĖłŗ¬ÓŠµÄÄÜĮæŌ½µĶ£¬ĪļÖŹµÄĪČ¶ØŠŌ¾ĶŌ½Ē攣ÓÉŹÆÄ«Öʱø½šøÕŹÆŹĒĪüČČ·“Ó¦”£Ņņ“ĖŃ”ĻīŹĒA”£
æ¼µć£ŗ漲齚øÕŹÆÓėŹÆÄ«µÄÄÜĮæ±Č½Ļ¼°Ļą»„×Ŗ»ÆŹ±µÄÄÜĮæµÄ¹ŲĻµµÄÖŖŹ¶”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
£Ø8·Ö£©Ń”ŌńŅŌĻĀĪļÖŹĢīŠ“ĻĀĮŠæÕ°×£ŗ
| A£®ĒāŃõ»ÆÄĘ | B£®Ńõ»ÆĆ¾ | C£®He | D£®¶žŃõ»Æ¹č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
¼×“¼ÖŹ×Ó½»»»Ä¤Č¼ĮĻµē³ŲÖŠ½«¼×“¼ÕōĘų×Ŗ»ÆĪŖĒāĘųµÄĮ½ÖÖ·“Ó¦ŌĄķŹĒ
¢ŁCH3OH(g)£«H2O(g)£½CO2(g)£«3H2(g) ?¦¤H £½£«49.0 kJ/mol
¢ŚCH3OH(g)£«1/2O2(g)£½CO2(g)£«2H2(g) ?¦¤H£½£192.9 kJ/mol
øł¾ŻÉĻŹö·“Ó¦£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ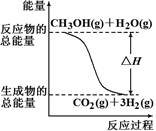
| A£®·“Ó¦¢ŁÖŠµÄÄÜĮæ±ä»ÆČēÉĻĶ¼ĖłŹ¾ |
| B£®æÉĶĘÖŖ2H2(g)£«O2(g)£½2H2O(g)?¦¤H£½£483.8 kJ/mol |
| C£®1 mol CH3OH³ä·ÖČ¼ÉշųöµÄČČĮæĪŖ192.9 kJ |
| D£®CH3OH×Ŗ±ä³ÉH2µÄ¹ż³ĢŅ»¶ØŅŖĪüŹÕÄÜĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
Ģ½¾æNaHCO3”¢Na2CO3ŗĶŃĪĖį(ŅŌĻĀŃĪĖįÅØ¶Č¾łĪŖ1 mol”¤L£1)·“Ó¦¹ż³ĢÖŠµÄČČŠ§Ó¦£¬ŹµŃé²āµĆČēĻĀŹż¾Ż£ŗ
| ŠņŗÅ | 35 mLŹŌ¼Į | ¹ĢĢå | »ģŗĻĒ° ĪĀ¶Č/”ę | »ģŗĻŗó ĪĀ¶Č/”ę |
| ¢Ł | Ė® | 2.5 g NaHCO3 | 20.0 | 18.5 |
| ¢Ś | Ė® | 3.2 g Na2CO3 | 20.0 | 24.3 |
| ¢Ū | ŃĪĖį | 2.5 g NaHCO3 | 20.0 | 16.2 |
| ¢Ü | ŃĪĖį | 3.2 g Na2CO3 | 20.0 | 25.1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠČČ»Æѧ·½³ĢŹ½ÖŠ£¬ÕżČ·µÄŹĒ£Ø £©
| A£®¼×ĶéµÄČ¼ÉÕČČĪŖ 890.3 kJ”¤mol-1£¬Ōņ¼×ĶéČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗ CH4£Øg£©+2O2£Øg£©=CO2£Øg£©+2H2O(g) ”÷H=-890£®3 kJ”¤mol-1 |
| B£®500”ę”¢30MPa ĻĀ£¬½« 0£®5mol N2£Øg£©ŗĶ 1£®5molH2£Øg£©ÖĆÓŚĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ӧɜ³É NH3£Øg£©·ÅČČ 19£®3 kJ£¬ĘäČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ N2£Øg£©+3H2£Øg£©  2NH3£Øg£© ”÷H = -38£®6 kJ”¤mol-1 2NH3£Øg£© ”÷H = -38£®6 kJ”¤mol-1 |
| C£®HCl ŗĶ NaOH ·“Ó¦µÄÖŠŗĶČČ”÷H =" -57.3" kJ”¤mol-1£¬ Ōņ H2SO4ŗĶ Ca£ØOH£©2·“Ó¦µÄÖŠŗĶČČ ”÷H = 2”Į£Ø-57£®3£©kJ”¤mol -1 |
| D£®ŌŚ 101 kPa Ź±£¬2gH2ĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®£¬·Å³ö 285£®8kJ ČČĮ棬ĒāĘųČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½±ķŹ¾ĪŖ 2H2(g)+O2(g)=2H2O£Ø1£©”÷H = -571£®6 kJ”¤mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
»Æѧ·“Ó¦A2 £« B2 £½ 2ABµÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )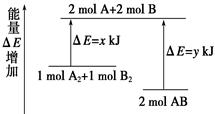
| A£®øĆ·“Ó¦ŹĒĪüČČ·“Ó¦ |
| B£®¶ĻĮŃ1 mol A”ŖA¼üŗĶ1 mol B”ŖB¼üÄܷųöx kJµÄÄÜĮæ |
| C£®¶ĻĮŃ2 mol A”ŖB¼üŠčŅŖĪüŹÕy kJµÄÄÜĮæ |
| D£®2 mol ABµÄ×ÜÄÜĮæøßÓŚ1 mol A2ŗĶ1 mol B2µÄ×ÜÄÜĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠ·“Ó¦¼ČŹĒŃõ»Æ»¹Ō·“Ó¦£¬ÓÖŹĒĪüČČ·“Ó¦µÄŹĒ£Ø £©
| A£®ĀĮʬŗĶĻ”ĮņĖį·“Ó¦ | B£®Ba£ØOH£©2?8H2OÓėNH4Cl·“Ó¦ |
| C£®×ĘČȵÄĢæÓėCO2·“Ó¦ | D£®¼×ĶéŌŚO2ÖŠČ¼ÉÕ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
Ī“Ą“ŠĀÄÜŌ“µÄĢŲµćŹĒ׏Ō“·įø»£¬ŌŚŹ¹ÓĆŹ±¶Ō»·¾³ĪŽĪŪČ¾»ņĪŪČ¾ŗÜŠ”£¬ĒŅæÉŅŌŌŁÉś”£ĻĀĮŠ·ūŗĻĪ“Ą“ŠĀÄÜŌ“±ź×¼µÄŹĒ(””””)
¢ŁĢģČ»Ęų””¢ŚĆŗ””¢ŪŗĖÄÜ””¢ÜŹÆÓĶ””¢ŻĢ«ŃōÄÜ””¢ŽÉśĪļÖŹÄÜ””¢ß·ēÄÜ””¢ąĒāÄÜ
| A£®¢Ł¢Ś¢Ū¢Ü | B£®¢Ż¢Ž¢ß¢ą | C£®¢Ū¢Ż¢Ž¢ß¢ą | D£®¢Ū¢Ü¢Ż¢Ž¢ß¢ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŦŌ¼Ņ»¼Ņ¹«Ė¾Éč¼Ę³öSoccket×ćĒņ£¬Ćæ±»ĢßŅ»ĻĀ£¬×ćĒņµÄÄŚÖĆ»śÖĘ¾Ķ»į°ŃÄÜĮæ“¢“ęĘšĄ“£»±»“¢“ęµÄÄÜĮææÉŅŌĶعżUSB½ÓæŚøųŹÖ»ś»ņĘäĖūŠ”¼Ņµē³äµē”£ŌŚSoccket×ćĒņ³ä·ÅµēµÄ¹ż³ĢÖŠ£¬ÄÜĮæ×Ŗ»ÆµÄÖ÷ŅŖŠĪŹ½ŹĒ
A£®µēÄÜ”ś »ÆѧÄÜ”śµēÄÜ B£®»ÆѧÄÜ”śµēÄÜ”ś»ÆѧÄÜ
C£¬»śŠµÄÜ”śµēÄÜ”ś»ÆѧÄÜ D£®»śŠµÄÜ”ś»ÆѧÄÜ”śµēÄÜ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com