

���� ��������Ҫ�ɷ�Fe2O3������������SiO2�����ʵ�������Ϊԭ���Ʊ���������ĩ��ʵ����ƣ���Ҫ����������ܹ��̼���ϡ�����ܽ���������������������������������ͨ����Һ�е�SO2���壬�õ�����Ͷ��������漰������ԭ��Ӧ�ķ��������ݴ�����
��1���ɽ��Ӱ�췴Ӧ���ʵ�����ȥ������߷�Ӧ�ٵķ�Ӧ���ʵķ�����
��2�����ں�������������Һ��ͨ��SO2���壬�����ķ�ӦΪ2Fe3++SO2+2H2O=2Fe2++SO42-+4H+�����ݷ�Ӧԭ��������ҺpH�½���ԭ��
�ڿɲο��¶ȶԶ������ܽ�ȵ�Ӱ��ȥ���ǣ�
��3�����̶��м�ͷ��ָ��ɿ����������˺����Һ�е���������¼���μӷ�Ӧ�٣��ɼ��ǿ�ѭ�����õ����ʣ�
��4�����յζ�ԭ����2Fe3++2I-=2Fe2++I2��2Na2S2O3+I2=Na2S4O6+2NaI����Fe3+��Na2S2O3�Ĺ�ϵʽ���м��㣮
��� �⣺��1�����Ӱ�췴Ӧ���ʵ����أ�����������ʱ����ͨ��������顢�����¶ȡ����衢��������Ũ������߷�Ӧ���ʣ�
�ʴ�Ϊ�������������顢�ʵ����������Ũ�ȡ������¶ȡ�����ȣ�
��2����Fe3+��SO2��ˮ��Һ��H2SO3������ΪH2SO4������Һ��pH�����٣�Ҳ������Һ��������ǿ��
�ʴ�Ϊ��Fe3+��SO2��ˮ��Һ��H2SO3������ΪH2SO4��
���¶����ߣ����Լӿ췴Ӧ���ʣ���������ܽ��ȴ��С�ˣ��μӷ�Ӧ��SO2�������٣�����ͬʱ���ڣ�T1�¶�����Һ��pH���ߣ�
�ʴ�Ϊ���¶ȹ��ߣ�SO2���ܽ���½���
��3��������ͼ�пɿ�������ѭ�����õ�������H2SO4��
�ʴ�Ϊ��H2SO4��
��4���ɷ�Ӧʽ�ɵù�ϵ��Fe3+��Na2S2O3��n��Fe3+��=n��Na2S2O3��=20.00��10-3 L��0.50mol/L��10=0.1 mol��
��c��Fe3+��=$\frac{0.1mol}{20.00��10{\;}^{-3}L}$=5.0mol/L��
��ԭ��Һ������Ũ��Ϊ5.0mol/L��
���� ���⿼������������ԭ��Ӧ�����۷���ʵ��ԭ�����漰Ӱ�췴Ӧ���ʵ����ؼ��ζ�ԭ�������ݴ������Ѷ��еȣ�


 ��ǰ�κ�ͬ����ϰϵ�д�
��ǰ�κ�ͬ����ϰϵ�д� ����С��ҵϵ�д�
����С��ҵϵ�д� �Ƹ�С״Ԫ����������ϰ��ϵ�д�
�Ƹ�С״Ԫ����������ϰ��ϵ�д� �ɹ�ѵ���ƻ�ϵ�д�
�ɹ�ѵ���ƻ�ϵ�д� ����ѵ����ֱͨ�п�����ϵ�д�
����ѵ����ֱͨ�п�����ϵ�д� һ���㶨ϵ�д�
һ���㶨ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ۢޢ� | B�� | �ڢۢޢ� | C�� | �ڢۢܢ� | D�� | �ڢۢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
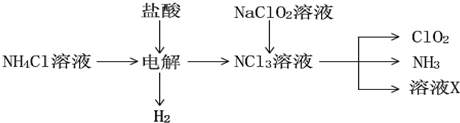
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
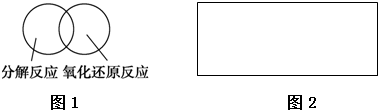
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
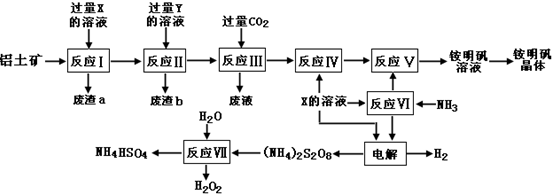
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���ж��������ʲ�����B������ѧ��Ӧ����C��
���ж��������ʲ�����B������ѧ��Ӧ����C���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2���ӵı���ģ�ͣ� | |
| B�� | ��������ĵ���ʽ��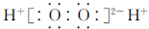 | |
| C�� | ��ԭ�ӵĽṹʾ��ͼ��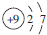 | |
| D�� | H2CO3�ĵ��뷽��ʽ��H2CO3?2H++CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
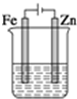
| A�� | ��Һ����������п�缫�ƶ� | B�� | п�缫�������������� | ||
| C�� | ���˵缫���������������� | D�� | ��·�е���ת����Ϊ0.4NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com