
| A、Fe(OH)3胶体有较强的吸附作用,是因为胶粒有较大的表面积 |
| B、白磷熔化、干冰汽化、SiO2熔化、AlCl3升华都是克服分子间作用力 |
| C、液晶是一种介于晶体和液体之间的中间态物质,分子较小,在信息技术中作用较大 |
| D、电解质熔融时一定能导电,因为破坏了化学键产生自由移动的离子 |
科目:高中化学 来源: 题型:
 离子交换膜是一类具有离子交换功能的高分子材料,在生产和科研中有广泛应用.一容器被离子交换膜分成左右两部分,如图所示:
离子交换膜是一类具有离子交换功能的高分子材料,在生产和科研中有广泛应用.一容器被离子交换膜分成左右两部分,如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1-2.25a% |
| B、2.25a% |
| C、1-1.75a% |
| D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol.L-1 |
| B、0.2mol.L-1 |
| C、0.4mol.L-1 |
| D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑥ | B、①④⑤ |
| C、③④ | D、②⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
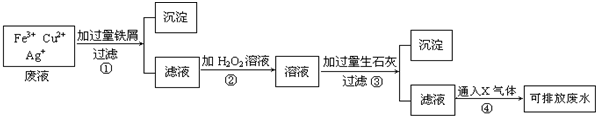
查看答案和解析>>
科目:高中化学 来源: 题型:
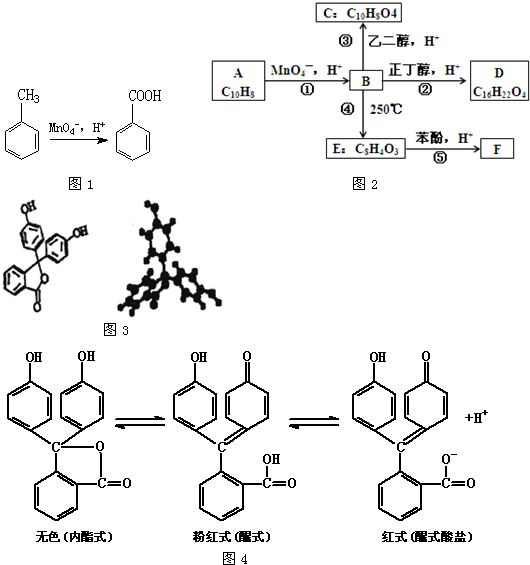
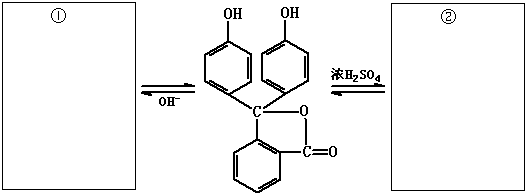
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com