
【题目】在一定温度下将1molCO 和3mol 水蒸气放在密闭的容器中发生下列反应CO(g)+H2O(g)CO2(g)+H2(g)达到平衡后,测得CO2为0.75mol,再通入6mol 水蒸气,达到新的平衡后,CO2和H2的物质的量之和为( )
A.1.2 mol
B.1.5 mol
C.1.8 mol
D.2.1 mol
【答案】C
【解析】解:到平衡后,测得CO2为0.75mol,则
CO+ | H2O(g) | CO2 + | H2 | ||
初始物质的量: | 1 | 3 | 0 | 0 | |
变化物质的量: | 0.75 | 0.75 | 0.75 | 0.75 | |
平衡物质的量: | 0.25 | 2.25 | 0.75 | 0.75 |
K= ![]() =1,
=1,
再通入6mol 水蒸气,化学平衡会向着正反应方向进行,相当于起始量为1molCO,9molH2O,设消耗一氧化碳物质的量为x,
则
CO+ | H2O(g) | CO2 + | H2 | ||
初始物质的量: | 1 | 9 | 0 | 0 | |
变化物质的量: | x | x | x | x | |
平衡物质的量: | 1﹣x | 9﹣x | x | x |
K= ![]() =1,
=1,
解得x=0.9,
则二氧化碳和氢气物质的量之和为0.9mol+0.9mol=1.8mol,
故选C.
到平衡后,测得CO2为0.75mol,则
CO+ | H2O(g) | CO2 + | H2 | ||
初始物质的量: | 1 | 3 | 0 | 0 | |
变化物质的量: | 0.75 | 0.75 | 0.75 | 0.75 | |
平衡物质的量: | 0.25 | 2.25 | 0.75 | 0.75 |
K= ![]() =1,
=1,
再通入6mol 水蒸气,化学平衡会向着正反应方向进行,但平衡常数随温度变化,不随浓度变化,以此计算.


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
【题目】有关乙炔分子中的化学键描述不正确的是( )
A.两个碳原子采用sp杂化方式
B.两个碳原子采用sp2杂化方式
C.每个碳原子都有两个未杂化的2p轨道形成π键
D.两个碳原子形成两个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冬天使用的热敷袋里面有铁粉、氯化钠、碳粉,利用铁被氧化放出的热量取暖.某同学拆开一袋后取里面的固体粉末进行实验:
①将粉末投入盛有足量稀盐酸的烧杯中,观察到有大量气泡产生,底部有黑色粉末.则发生反应的离子方程式为 .
②为分离出反应后的溶液,可将上述烧杯中混合物进行操作,该操作需要的玻璃仪器为 .
③在②得到的溶液中通入氯气,发生如下离子反应:2Fe2++Cl2=2Fe3++2Cl-;在该离子方程式中,当有ag氧化产物生成时,需通入标准状况下的氯气体积为L(用含a的代数式表示).
④该同学将少量铜片投入制得的含FeCl3的溶液中,发现铜片慢慢溶解消失,溶液由黄色变为青绿色.则发生反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO、CO2是火力发电厂释放出的主要尾气,为减少对环境造成的影响,发电厂试图采用以下方法将其资源化利用,重新获得燃料或重要工业产品.
(1)CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2 , 在催化剂的作用下发生反应:CO(g)+Cl2(g)COCl2(g)△H=a kJ/mol反应过程中测定的部分数据如下表:
t/min | n (CO)/mol | n (Cl2)/mol |
0 | 1.20 | 0.60 |
1 | 0.90 | |
2 | 0.80 | |
4 | 0.20 |
①反应0~2min末的平均速率v(COCl2)=mol/(Lmin).
②在2min~4min间,v(Cl2)正 v(Cl2)逆 (填“>”、“=”或“<”),该温度下K=
③已知X、L可分别代表温度或压强,图1表示L一定时,CO的转化率随X的变化关系.
X代表的物理量是;a0 (填“>”,“=”,“<”).
(2)在催化剂作用下NO和CO转化为无毒气体,2CO(g)+2NO(g)2CO2(g)+N2(g)△H=﹣748kJmol﹣1
①一定条件下,单位时间内不同温度下测定的氮氧化物转化率如图2所示.温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是 .
②已知:测定空气中NO和CO含量常用的方法有两种,方法1:电化学气敏传感器法.其中CO传感器的工作原理如图3所示,则工作电极的反应式为;方法2:氧化还原滴定法.用H2O2溶液吸收尾气,将氮氧化物转化为强酸,用酸碱中和滴定法测定强酸浓度.写出NO与H2O2溶液反应的离子方程式
(3)用CO和H2可以制备甲醇,反应为CO(g)+2H2(g)CH3OH(g),以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)若电解质溶液中KOH的物质的量为0.8mol,当有0.5mol甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中所含分子物质的量最多的是( )
A. 56 g N2 B. 标准状况下3.36 L O2
C. 6 g H2 D. 3.01×1023个H2SO4分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度为1molL﹣1的是( )
A.将40 g NaOH溶于1 L水所得的溶液
B.将22.4 L HCl溶于水配成1 L溶液
C.1 L含2 mol K+的K2SO4溶液
D.将0.5 molL﹣1的NaNO3溶液100 mL加热蒸发掉50 g 水后的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=2的A,B两种酸溶液各1mL,分别加水稀释到1000mL,其中pH与溶液体积V的关系如图所示.下列说法正确的是( ) 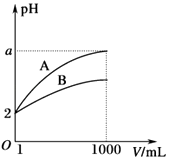
A.A,B两酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液强
C.a=5时,A是强酸,B是弱酸
D.若a小于5,则A,B都是弱酸,且A的酸性弱于B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列物质中,其物质的量为0.2mol的是( )
A. 2.2g CO2 B. 3.6g H2O C. 3.2g O2 D. 49g H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核电荷数为16的元素和核电荷数为4的元素的原子相比较,前者下列数据是后者4倍的是( )
①电子数 ②最外层电子数 ③电子层数 ④次外层电子数
A. ①④B. ①③④C. ①②④D. ①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com