
| A. | 通入Cl2后,溶液变为黄色,加淀粉液后溶液变蓝,则原溶液中一定有I- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液中一定有SO42- | |
| C. | 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32- | |
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状态下的辛烷22.4L完全燃烧产生CO2分子数为8NA | |
| B. | 18克水所含的电子数为10NA | |
| C. | 46克NO2和46克N2O4中所含原子数均为3NA | |
| D. | 1L2molL的Mg(NO3)2溶液中含NO3个数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 设锌镀层厚度为h,锌的密度为ρ,则$\frac{{{m_1}-{m_2}}}{ρS}$=h | |
| B. | 锌电极上发生还原反应 | |
| C. | 锌和石墨形成原电池,外电路中电流从锌流向石墨 | |
| D. | 当石墨不再产生气泡时,应立即取出铁皮 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 L1mol/L NaHS溶液中,N(Na+)+N(HS-)=NA | |
| B. | 12.4g白磷(分子式为P4)中含有P-P共价键0.6NA | |
| C. | 常温下,pH=2的醋酸溶液中所含有的H+数为0.01NA | |
| D. | 将92gN2O4晶体放入容器中,恢复到常温常压时,所含气体分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定有SO32-离子 | B. | 不一定有CO32-离子 | ||
| C. | 不能确定Cl-离子是否存在 | D. | 不能确定HCO3-离子是否存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种元素中,元素Z的非金属性最强 | |
| B. | X、Y、Z三种元素不可能形成离子化合物 | |
| C. | Y、Z、W三种元素的原子半径大小顺序:r(W)>r(Z)>r(Y) | |
| D. | YW3、ZW2、Z2W2中各原子最外层均达到8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
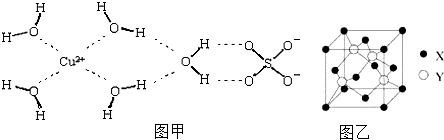
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
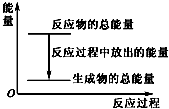
| A. | 反应过程中的能量关系可用如图表示 | |
| B. | 1 mol Zn的能量大于1 mol H2的能量 | |
| C. | 若将其设计为原电池,则锌作正极 | |
| D. | 若将其设计为原电池,当有32.5 g Zn溶解时,正极放出的气体一定为11.2 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com