
| 步骤 | 检验离 子 | 检验方法 | 现象 | 离子方程式 |
| Ⅰ | ① | 焰色反应 | 火焰呈紫色(透过蓝色钴玻璃) | |
| Ⅱ | Al3+ | 将氢氧化钠溶液逐滴加入到明矾溶液止过量 | ②先观察到: | Al3++3OH-=Al(OH)3↓ |
| 后观察到: | ③ | |||
| Ⅲ | SO42- | ④先加 | 无明显现象 | |
| 后加 | 产生白色沉淀 | Ba2++SO42-=BaSO4↓ |


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案科目:高中化学 来源: 题型:
| A、H+、K+、HCO3-、Ca2+ |
| B、OH-、Na+、Mg2+、HCO3- |
| C、Na+、SiO32-、H+、Cl- |
| D、K+、H+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
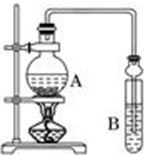 已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2?6C2H5OH;
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2?6C2H5OH;| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点(℃) | 34.5 | 78.3 | 118 | 77.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg2+、K+、Cl-、NO3- |
| B、OH-、Cl-、Na+、NH4+ |
| C、H+、K+、Fe2+、NO3- |
| D、I-、Cl-、H+、Fe3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com