
【题目】一定条件下的可逆反应2SO2+O2![]() 2SO3,下列判断能说明达到化学反应的限度的是
2SO3,下列判断能说明达到化学反应的限度的是
A.SO2完全转化为SO3
B.SO2、O2与SO3的物质的量之比为2∶1∶2
C.反应混合物中,SO3的质量分数不再改变
D.消耗2 mol SO2的同时生成2 mol SO3
【答案】C
【解析】
试题分析:A、可逆反应中反应物不能完全转化为生成物,A错误;B、SO2、O2与SO3的物质的量之比为2∶1∶2不能说明正逆反应速率相等,反应不一定达到平衡状态,B错误;C、反应混合物中,SO3的质量分数不再改变,说明反应达到平衡状态,C正确;D、消耗2 mol SO2的同时生成2 mol SO3均不是正反应速率,不能说明反应达到平衡状态,D错误,答案选D。
【名师点晴】在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。注意可逆反应达到平衡状态有两个核心的判断依据:①正反应速率和逆反应速率相等。②反应混合物中各组成成分的百分含量保持不变。只要抓住这两个特征就可确定反应是否达到平衡状态,对于随反应的发生而发生变化的物理量如果不变了,即说明可逆反应达到了平衡状态。判断化学反应是否达到平衡状态,关键是看给定的条件能否推出参与反应的任一物质的物质的量不再发生变化。


科目:高中化学 来源: 题型:
【题目】已知:4NH3+5O2=4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列关系正确的是
A. 4v(NH3)=5v(O2) B. 5v(O2)=6v(H2O)
C. 3v(NH3)=2v(H2O) D. 5v(O2)=4v(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种短周期元素,其中B,C、D、E四种元素在化学反应中均能形成简单的阴、阳离子,且B、C、D离子具有相同的电子层结构。已知:
①A是形成物质种类最多的元素,F和A同主族;
②C的氢化物分子G是具有10电子的微粒,且可以发生下图转化:
![]()
③E和D是同主族元素;
④B和D可形成个数比为1:1和2:1的离子化合物X和Y。
请回答下列问题:
(1)B与D形成离子化合物Y具有漂白性,写出Y的电子式______,该化合物和元素A的最高价氧化物O反应的化学方程式为:__________;一定量的Y与O反应后得到的固体物质,能恰好与含400 mL 2 mol/L的稀盐酸反应,并收集到0.25 mol气体,则该固体物质的组成为________(用物质的量表示)。
(2)G气体的检验方法为_________;13.44 L气体G(标准状况下测定)按照上图转化方式可以获得M物质的量分别为__________mol。
(3)某化学兴趣小组欲采用右图装置证明A、C、F三种元素性质的递变性,其中甲装置中锥形瓶内所加试剂为石灰石:
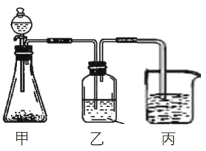
①甲装置中发生反应的离子方程式为________________;
②乙装置中应添加的试剂为______________;
③丙装置中可能发生的实验现象为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨分子中的一个氢原子被甲基取代后,所得甲胺(CH3NH2)的性质与氨相似,CH3NH2·H2O也是一元弱碱,25℃时电离常数Kb=4.0×10-5。现用0.0500mol/L的稀硫酸滴定l0mL 0.1000mol/L的甲胺溶液,溶液中c(OH-)的负对数(pOH)与所加稀硫酸的体积(V)的关系如图所示。下列说法正确的是
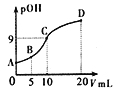
A. 甲胺在水中的电离方程式为:CH3NH2·H2O=CH3NH3++OH-
B. A、B、C三点溶液中,水电离出来的c(H+):B>C>A
C. C点所在溶液中![]()
D. B点溶液中存在c(CH3NH2·H2O)>c(CH3NH3+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,德国科学家利用数亿个镍原子(28Ni)对数亿个铅原子(82Pb)连续轰击数天后,制得一种新原子![]() (暂用X表示),它属于一种新元素——第110号元素,这种新元素是有史以来制得的最重的元素,存在时间不到千分之一秒,经分析它属于过渡元素,下列关于该元素的叙述中正确的是( )
(暂用X表示),它属于一种新元素——第110号元素,这种新元素是有史以来制得的最重的元素,存在时间不到千分之一秒,经分析它属于过渡元素,下列关于该元素的叙述中正确的是( )
A. 这种原子(![]() )的中子数为169
)的中子数为169
B. 这种元素肯定是金属元素
C. 这种元素属于第6周期元素
D. 这种元素与铅(82Pb)同族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1 mol的镁、铝混合物溶于100 mL 2mol/L H2SO4溶液中,然后再滴加1 mol/L NaOH溶液。请回答:
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如下图所示。

当V1=160mL时,则金属粉末中n(Mg)=________ mol,V2=_____________mL。
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH) _____________mL。
(3)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家预测原子序数为114的元素具有相当稳定的同位素,它的位置是在第七周期、第ⅣA族,称为“类铅”,关于它的性质的预测错误的是( )
A.它的原子最外层有4个电子
B.它具有+2、+4价
C.金属铜能从114号元素的硝酸盐溶液中置换出该元素的单质
D.它的金属性比铅强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com