
| A. | 混合气体密度恒定不变 | B. | 混合气体的颜色不再改变 | ||
| C. | H2、I2、HI 的浓度相同 | D. | I2在混合气体中体积分数不变 |
分析 可逆反应H2(g)+I2(g)?2HI(g)达到平衡状态时,正逆反应速率相等,各组分的浓度、百分含量不再变化,混合气体中只有碘单质为有色物质,混合气体颜色不变时,表明各组分浓度不变,达到平衡状态,据此进行解答.
解答 解:A.该反应气体都是气体,气体质量不变,气体的总体积也不变,则混合气体的密度始终不变,不能根据密度判断平衡状态,故A错误;
B.混合气体中只有碘单质有色,当混合气体颜色不变时,表明正逆反应速率相等,各组分浓度不再变化,达到了平衡状态,故B正确;
C.H2、I2、HI 的浓度相同时,无法判断各组分的浓度是否不再变化,无法判断是否达到平衡状态,故C错误;
D.I2在混合气体中体积分数不变,表明各组分的浓度不再变化,该反应达到平衡状态,故D正确;
故选BD.
点评 本题考查了化学平衡状态的判断,题目难度不大,明确化学平衡状态的特征为解答关键,注意达到平衡状态时各组分的浓度不再变化,而不一定相等,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 2SO2(g)+02(g) $?_{500℃}^{V_{2}O_{5}}$2SO3(g)△H=-196.6 kJ/mol,则2molSO2完全反应放出热量等于196.6kJ | |
| B. | “冰,水为之,而寒于水”说明相同质量的水和冰相比较,冰的能量高 | |
| C. | 已知C(s,石墨)=C(s,金刚石)△H=+1.9 kJ/mol,则金刚石比石墨稳定 | |
| D. | 氢气的燃烧热为285.8 kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
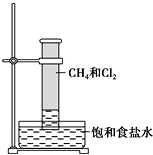 某课外活动小组利用如图所示装置探究甲烷与氯气的反应.根据题意,回答下列问题:
某课外活动小组利用如图所示装置探究甲烷与氯气的反应.根据题意,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在101 k Pa时,1 mol C与适量O2反应生成1mol CO时,放出110.5 kJ热 量,则C的燃烧热为110.5 kJ/mol | |
| B. | 在10l k Pa时l mol H2完全燃烧生成液态水放出285.8 kJ热量,H2燃烧热为-285.8KJ/mol | |
| C. | 鉴定HCl和NaOH反应的中和热时,每次实验均应测量3个温度即盐酸起始温度、NaOH起始温度和反应后终止温度 | |
| D. | 在稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-57.3KJ/mol,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量等于57.3KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在银锌原电池中,以硫酸铜为电解质溶液,锌为负极,电极上发生的是(“氧化”或“还原”)氧化反应,银电极上的电极反应式为Cu2++2e-═Cu.
在银锌原电池中,以硫酸铜为电解质溶液,锌为负极,电极上发生的是(“氧化”或“还原”)氧化反应,银电极上的电极反应式为Cu2++2e-═Cu.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4和C2H6 | B. | C2H4和C3H6 | C. | C2H6和C3H6 | D. | C2H4和C3H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
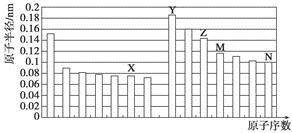
| A. | Z、N两种元素的离子半径相比,前者较大 | |
| B. | X、N两种元素的气态氢化物的沸点相比,前者较低 | |
| C. | 由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应 | |
| D. | Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com