
【题目】在水溶液中能大量共存的离子组是( )
A. Ba2+、H+、HCO3-、Cl- B. Cu2+、OH-、NH4+、Cl-
C. Ag+、NO3-、Cl-、H+ D. Na+、NO3-、SO42-、H+
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
【题目】除去括号内杂质所用试剂和方法不正确的是
A. CO2(HCl)——氢氧化钠溶液,洗气
B. KNO3(NaCl)——结晶
C. 水(NaCl)——蒸馏
D. Cu(Fe)——溶于足量盐酸,过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L恒容密闭容器中充入2 mol X和1mol Y发生反应:2X(g)+Y(g) ![]() 3Z(g) ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( )
3Z(g) ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( )

A. Q点时,Y的转化率最大
B. W点X的正反应速率等于M点X的正反应速率
C. 升高温度,平衡常数增大
D. 温度一定,平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冶炼金属一般有下列四种方法:①焦炭法;②水煤气(或氢气或一氧化碳)法;③活泼金属置换法;④电解法。四种方法在工业上均有应用,古代有(1)火烧孔雀石炼铜;(2)湿法炼铜;现代有(3)铝热法炼铬;(4)从光卤石(KCl·MgCl2·6H2O)中炼镁。对它们的冶炼方法的分析不正确的是( )
A.(1)用①B.(2)用②C.(3)用③D.(4)用④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
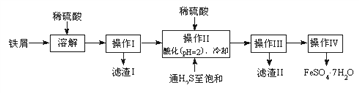
查询资料,得有关物质的数据如下表:
25℃时 | 饱和H2S溶液 | SnS沉淀完全 | FeS开始沉淀 | FeS沉淀完全 |
pH值 | 3.9 | 1.6 | 3.0 | 5.5 |
(1)检验制得的绿矾晶体中是否含有Fe3+,最好选用的试剂为____________________。
A.KSCN溶液B.NaOH溶液C.KMnO4溶液
(2)操作II中,通入硫化氢至饱和的目的是(写两点)___________、____________。
(3)操作IV的顺序依次为________、冷却结晶、过滤。
(4)测定绿矾产品中Fe2+含量的方法是:
a.称取3.72g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①滴定时盛放KMnO4溶液的仪器为_________(填仪器名称)。
②计算上述样品中FeSO47H2O的质量分数为__________。
③上述测定中,若滴定管规格为50mL,则步骤a中称取样品的质量不能超过______g。(保留4位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气阴极祛制备H2O2是一种环境友好型制备方法,装置如图所示,下列说法错误的是
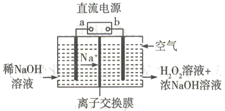
A. b为直流电源的负极
B. 本装置使用的交换膜为阳离子交换膜
C. 通入空气的电极反应式可能为O2+2e-+2H2O=H2O2+2OH-
D. 若生成17g双氧水,则需要通入含11.2 LO2 的空气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学学习中使用数轴的表示方法可起到直观、形象的效果,下列表达中不正确的是( )
A. 常温下溶液的pH与酸碱性的关系: ![]()
B. Fe在Cl2中的燃烧产物: 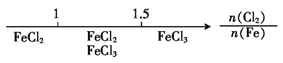
C. 硫的化合物中化合价与其氧化性、还原性的关系: 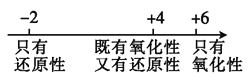
D. 氨水与SO2反应后溶液中的铵盐: 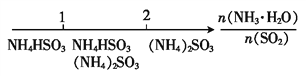
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
①燃料电池的反应物可不储存在电池的内部
②锌锰干电池是一次电池,铅蓄电池是二次电池
③锂电池是新一代可充电电池
④燃料电池作为汽车驱动能源已研发成功
A.②③④B.①②③④
C.①②③D.①③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com