
分析 (1)H3PO2是一元中强酸,在水溶液里部分电离生成氢离子和酸根离子;
(2)①根据化合物中化合价的代数和为0确定P元素化合价;
②根据转移电子守恒判断氧化产物;
③H3PO2是一元中强酸,则NaH2PO2为正盐,酸根离子在水溶液里水解导致溶液呈碱性.
解答 解:(1)H3PO2是一元中强酸,在水溶液里部分电离生成氢离子和酸根离子,电离方程式为H3PO2?H++H2PO2-,
故答案为:H3PO2?H++H2PO2-;
(2)①根据化合物中化合价的代数和为0确定P元素化合价,O元素为-2价、H元素为+1价,所以P元素为+1价,故答案为:+1;
②该反应中银离子是氧化剂、H3PO2是还原剂,氧化剂与还原剂的物质的量之比为4:1,根据转移电子相等知,1molH3PO2失去4mol电子,所以P元素为+5价,则氧化产物是H3PO4,故答案为:H3PO4;
③H3PO2是一元中强酸,则NaH2PO2为正盐,酸根离子在水溶液里水解导致溶液呈碱性,
故答案为:正盐;弱碱性.
点评 本题考查氧化还原反应、电离方程式的书写、盐类水解等知识点,明确物质的性质是解本题关键,利用守恒思想、电离方程式书写规则、盐类水解原理解答即可,题目难度不大.


科目:高中化学 来源:2017届黑龙江省哈尔滨市高三上学期期中考试化学试卷(解析版) 题型:实验题
某小组同学以碳棒为电极电解CuCl2溶液时,发现阴极碳棒上除了有红色物质析出外,还有少量白色物质析出。为探究阴极碳棒上的产物,同学们阅读资料并设计了如下过程:
Ⅰ.有关资料:铜的化合物颜色性质如下
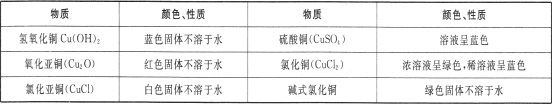
Ⅱ.探究实验:
(1)提出假设
①红色物质一定有铜,还可能有Cu2O;
②白色物质为铜的化合物,其化学式可能为。
(2)实验验证
取电解CuCl2溶液后的阴极碳棒,洗 涤、干燥,连接下列装置进行实验,验证阴极产物,
涤、干燥,连接下列装置进行实验,验证阴极产物,
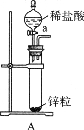
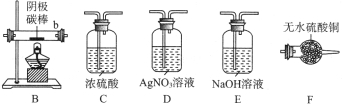
①实验前,检查装置A气密性的方法是。
②实验 时,各装置从左至右的连接顺序为A→→→B→→。
时,各装置从左至右的连接顺序为A→→→B→→。
(3)观察现象,得出结论
实验结束后,碳棒上的白色物质变为红色,F中物质不变色,D中出现白色沉淀,根据现象①碳棒上的红色物质是否有Cu2O(填“是”或“否”),理由是;②装置(填上图中装置编号)中的现象说明提出假设②中的白色物质一定存在;③写出装置b中发生反应的化学方程式。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.2g | B. | 8.4g | C. | 16.8g | D. | 22.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中:Na+、K+、MnO4-、CO32- | |
| B. | c(H+)=1×10-13mol/L的溶液中:Mg2+、Cu2+、SO42-、NO3- | |
| C. | 0.1mol/LNH4HCO3溶液中:K+、Na+、NO3-、Cl- | |
| D. | 0.1mol/LFeCl3溶液中:Fe2+、NH4+、SCN-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
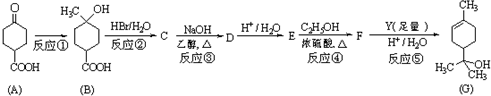
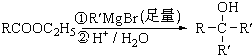
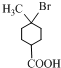 +2NaOH
+2NaOH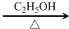
 +NaBr+2H2O.
+NaBr+2H2O.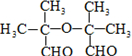 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知反应:2N02 (红棕色)?N204 (无色)△H<0.将一定量的N02充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法正确的是( )
已知反应:2N02 (红棕色)?N204 (无色)△H<0.将一定量的N02充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法正确的是( )| A. | b点的操作是压缩注射器 | |
| B. | c点与a点相比,c(NO2)增大,c(N2O4)减小 | |
| C. | 若不忽略体系温度变化,且没有能量损失,则 r(b)>r(c) | |
| D. | d 点:v(正)>v(逆) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 有机物A分子的结构简式为
有机物A分子的结构简式为 ;
; ;
; .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com