
| A.浓氨水 | B.纯水 |
| C.少量K2CO3固体 | D.少量浓H2SO4 |
科目:高中化学 来源:不详 题型:单选题
| A.V2=10V1 | B.V1<10 V2、 | C.10V1>V2 | D.V2>10V1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H++F-。25℃下,向20mL0.2mol?L-1的氢氟酸中滴加0.2mol?L-1的NaOH溶液时,溶液的pH变化如图所示。
H++F-。25℃下,向20mL0.2mol?L-1的氢氟酸中滴加0.2mol?L-1的NaOH溶液时,溶液的pH变化如图所示。
 )和电离平衡常数(K)一样,可以用来衡量弱电解质在稀溶液中的电离能力,
)和电离平衡常数(K)一样,可以用来衡量弱电解质在稀溶液中的电离能力, 。
。 (HF)]增大的是_______,可使氢氟酸的电离平衡常数[Ka(HF)] 增大的是_______。
(HF)]增大的是_______,可使氢氟酸的电离平衡常数[Ka(HF)] 增大的是_______。 约为___ _%。
约为___ _%。 H+(aq)+F-(aq) △H=+b kJ?mol -1
H+(aq)+F-(aq) △H=+b kJ?mol -1 = Ka(HF)
= Ka(HF)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
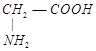 ,其中既能跟盐酸,又能跟NaOH溶液反应的有
,其中既能跟盐酸,又能跟NaOH溶液反应的有 | A.只有②④ | B.只有①② | C.只有①②③ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.H2S 2H+ + S2- 2H+ + S2- | B.HClO = H+ +ClO- |
C.CH3COONH4 NH4+ +CH3COO- NH4+ +CH3COO- | D.HCO3—+H2O  H3O++CO32- H3O++CO32- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com