
| A、1:2:3 |
| B、6:3:2 |
| C、1:1:1 |
| D、2:1:1 |
| 1 |
| 2 |


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、都呈透明的红褐色 |
| B、都比较稳定,密封保存一段时间都不会产生沉淀 |
| C、分散质颗粒直径相同 |
| D、当有光线透过时,都能产生丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
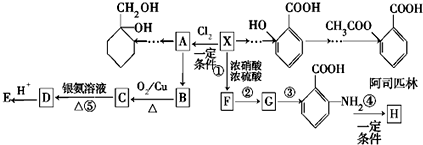

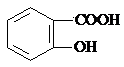 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物,其核磁共振氢谱图中峰面积之比为1:2:2:1,则符合上述条件的所有同分异构体的结构简式是
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物,其核磁共振氢谱图中峰面积之比为1:2:2:1,则符合上述条件的所有同分异构体的结构简式是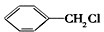 和其他无机物合成
和其他无机物合成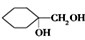 的最合理的方案(不超过4步).例如:
的最合理的方案(不超过4步).例如: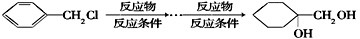
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、这种饮料中不含任何化学物质 |
| B、这种蒸馏水绝对纯净,其中不含任何离子 |
| C、这种口服液含丰富的N、P、Zn等微量元素 |
| D、没有水就没有生命 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com