
某硫酸铜晶体CuSO4·nH2O m g加热至失去全部结晶水后,测得剩余固体的质量为w g,则n的计算式为( )
A.![]() B.
B.![]()
C.![]() D.无法计算
D.无法计算
科目:高中化学 来源: 题型:
(1)使用铜和稀硫酸制备硫酸铜晶体?
步骤如下:?
![]()
步骤①观察到的现象是 。?
步骤③的主要操作包括: 。
(2)某硫酸铜晶体(CuSO4·nH2O)中含有少量的氯化钠,实验室里测定结晶水n的数值?
A.在实验过程中要用到下列仪器中的 (填序号,下同)。?
①容量瓶 ②托盘天平 ③烧杯 ④锥形瓶 ?⑤漏斗? ⑥干燥器 ⑦长颈漏斗 ⑧试管 ⑨试管夹 ?⑩坩埚?
B.在下列操作中,选用必要的步骤,按操作先后顺序排列 。?
①称量硫酸铜晶体 ②加水溶解 ③过滤 ④加过量AgNO3溶液 ⑤称出加热后固体质量 ⑥加热⑦加过量BaCl2溶液 ⑧称量沉淀?
C.在以上操作中,若硫酸铜晶体质量为a g,沉淀质量为b g,加热后固体质量为c g,则a g硫酸铜晶体中结晶水n为 。?
(3)硫酸铜溶解度的测定?
用石墨电极(相同)电解饱和CuSO4溶液,阴极的电极反应式是 。
已知饱和CuSO4溶液的质量为60 g,通电10 min后,溶液恰好变为无色。称量发现两电极质量差为4 g,此温度下CuSO4的溶解度是 。?
(4)已知铜屑放入稀硫酸中不发生反应,若在稀硫酸中加入H2O2,铜屑可逐渐溶解。请写出该反应的化学方程式: 。?
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学用含硫酸亚铁等杂质的工业硫酸铜制取纯净的氧化铜以探究其性质。
(1)制备氧化铜
①将工业硫酸铜加适量水溶解、搅拌、过滤除去不溶性杂质。简述检验滤液中含有Fe2+的操作方法: 。
②向滤液中滴加H2O2溶液,稍加热,当Fe2+转化完全后,为将Fe3+全部转化为Fe(OH)3沉淀,而不会将Cu2+转化为沉淀,需慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制溶液pH=3.5。加热煮沸后过滤,用稀硫酸酸化滤液至pH=1。再从溶液中分离出硫酸铜晶体。Fe2+转化为Fe3+的离子方程式是 。
③在测定所得硫酸铜晶体(CuSO4·xH2O)x值的实验中,所用的玻璃仪器名称为:酒精灯、
玻璃棒、 ,实验过程中称量操作至少进行 次。
④用得到的硫酸铜晶体制氧化铜。
(2)探究氧化铜的性质
在加热条件下,向下图所示装置中持续通入某纯净物X的蒸气,a处黑色物质变为红色,b处白色粉末变为蓝色,c处有无色液体产生。(设各步反应均进行完全)
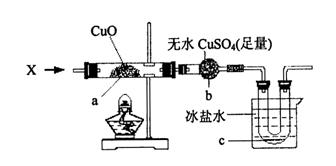
则X可能是 (填一个化学式即可),X与CuO反应的化学方程式是
。
查看答案和解析>>
科目:高中化学 来源:2012届北京市顺义区高三尖子生综合素质展示化学试卷 题型:实验题
(10分)常温下,某工厂以浓硫酸、浓硝酸、粗铜、水和空气为原料,设计如图所示制取硫酸铜晶体(CuSO4·5H2O)的生产工序和流程。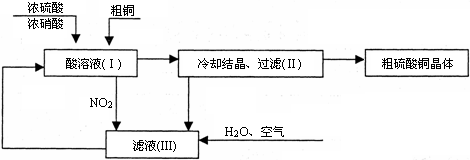
回答下列问题:
(1)(I)中制取硫酸铜的总反应的化学方程式为 。
(2)在上述反应中可以被循环利用的物质为 (写化学式)。
(3)①某同学在实验室中模拟上述生产过程实现上述方案,请根据该同学的思路在下列装置中选用适当的装置,并将它们的编号填入方框内。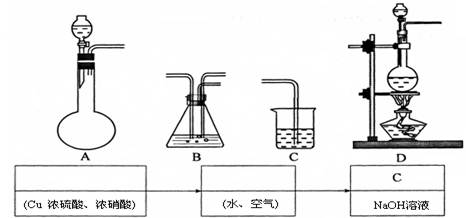
②装置C的作用是 。
(4)硫酸铜晶体也可以直接用浓硫酸和粗铜反应制取,与上述方法相比,其缺点是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com