
(14分)(Ⅰ)、A、B、C、D、E、五种元素均是短周期元素,且原子序数依次增大。B、E原子的最外层电子数均为其电子层数的2倍。D、E元素原子的最外层电子数相等。X、Y、Z、W、G、甲、乙七种物质均由上述中的两种或三种元素组成。元素B形成的单质M与甲、乙(相对分子质量:甲<乙)浓溶液的反应分别是:甲与M反应生成X、Y、Z,乙与M反应生成Y、Z、W,反应条件均省略。回答下列有关问题:
⑴X、Y、W均能与Z反应,若将标准状况下的X和D2按4:1充满试管后将其倒立于水槽中,待水不在上升时,试管内溶质的物质的量浓度是 (假设溶质不扩散)
⑵若将X、W、D2按4:4:3通入Z中充分反应,写出总的离子方程式
⑶G是一种既能与强酸又能与强碱反应的酸式盐,则G的电子式 ,取0.2mol/L的NaOH溶液与0.1mol/L的G溶液等体积混合后,加热至充分反应后,待恢复至室温剩余溶液中离子浓度的由大到小顺序是 ,此时测得溶液的PH=12,则此条件下G中阴离子的电离平衡常数Ka =
(Ⅱ)⑷某温度时,向AgNO3溶液中加入K2CrO4溶液会生成
Ag2CrO4沉淀,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。
该温度下,下列说法正确的是_________。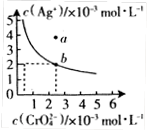
A. Ag2CrO4的溶度积常数(Ksp)为1×10-8
B. 含有大量CrO 的溶液中一定不存在Ag+
的溶液中一定不存在Ag+
C. a点表示Ag2CrO4的不饱和溶液,蒸发可以使溶液由a点变到b点
D. 0.02mol·L-1的AgNO3溶液与0.02mol·L-1的Na2CrO4溶液等体积混合会生成沉淀
⑸若常温下Ksp[Cr(OH)3]=10-32,要使c(Cr3+)降至10-5mol·L-1,溶液的pH应调至_______。
(14分,每空2分)Ⅰ 1/28mol/L 4NO2+4SO2+3O2+6H2O==4NO3-+4SO42-+12H+ 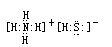
CNa+>CS2->COH->CHS->CH+ 4×10-12mol/L,
Ⅱ.AD 5
解析试题分析:I、B、E原子的最外层电子数均为其电子层数的2倍,所以B是C元素,E是S元素;D、E元素原子的最外层电子数相等,D与E同主族,所以D是O元素;则A、C分别是H、N元素。C单质可与浓硫酸、浓硝酸反应,则甲是硝酸,乙是硫酸,二者的共同产物是CO2、H2O,C与浓硝酸反应还原产物是NO2,与浓硫酸反应还原产物是SO2,所以X是NO2,W是SO2。
(1)X、Y、W均能与Z反应,说明Z是H2O,Y是CO2,NO2与O2按4:1充满试管后将其倒立于水槽中,二者恰好完全反应生成硝酸,溶液充满整个试管,设试管体积为VL(标准状况),则NO2的体积为0.8VL,生成的硝酸的物质的量是0.8VL/22.4L/mol,所得硝酸溶液的浓度是0.8VL/22.4L/mol/VL=1/28mol/L;
(2)将NO2、SO2、O2按4:4:3通入水中,恰好发生氧化还原反应,生成硝酸和硫酸,离子方程式为4NO2+4SO2+3O2+6H2O==4NO3-+4SO42-+12H+;
(3)G是一种既能与强酸又能与强碱反应的酸式盐,且由2种或3种元素构成,所以G是NH4HS,电子式为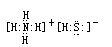 ;氢氧化钠与硫氢化铵在加热条件下以物质的量比2:1反应生成硫化钠、氨气,硫离子水解,使溶液显碱性,所以溶液中离子浓度从大到小的顺序是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+);混合溶液中c(S2-)=0.05mol/L,溶液pH=12,则c(H+)=1×10-12mol/L,c(OH-)= 1×10-2mol/L,根据S2-+H2O
;氢氧化钠与硫氢化铵在加热条件下以物质的量比2:1反应生成硫化钠、氨气,硫离子水解,使溶液显碱性,所以溶液中离子浓度从大到小的顺序是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+);混合溶液中c(S2-)=0.05mol/L,溶液pH=12,则c(H+)=1×10-12mol/L,c(OH-)= 1×10-2mol/L,根据S2-+H2O HS-+OH-,所以c(HS-)= c(OH-)= 1×10-2mol/L,此时c(S2-)="0.05mol/L-0.01mol/L=0.04mol/L," 所以HS-的电离平衡常数Ka= c(H+) c(S2-)/ c(HS-)=4×10-12mol/L;
HS-+OH-,所以c(HS-)= c(OH-)= 1×10-2mol/L,此时c(S2-)="0.05mol/L-0.01mol/L=0.04mol/L," 所以HS-的电离平衡常数Ka= c(H+) c(S2-)/ c(HS-)=4×10-12mol/L;
II、(4)A、图像上的任何点都表示Ag2CrO4的溶解平衡时的离子浓度,所以溶度积常数=c(Ag+)2×c(CrO )=(2×10-3)2×2.5×10-3=1×10-8,正确;B、因为存在沉淀的溶解平衡,所以含有大量CrO
)=(2×10-3)2×2.5×10-3=1×10-8,正确;B、因为存在沉淀的溶解平衡,所以含有大量CrO 的溶液中也可能存在Ag+,错误;C、a点的离子浓度积大于b点溶解平衡常数,所以溶液为过饱和溶液,有沉淀析出,错误;D、0.02mol·L-1的AgNO3溶液与0.02mol·L-1的Na2CrO4溶液等体积混合,c(Ag+)= c(CrO
的溶液中也可能存在Ag+,错误;C、a点的离子浓度积大于b点溶解平衡常数,所以溶液为过饱和溶液,有沉淀析出,错误;D、0.02mol·L-1的AgNO3溶液与0.02mol·L-1的Na2CrO4溶液等体积混合,c(Ag+)= c(CrO )=0.01mol/L,则c(Ag+)2×c(CrO
)=0.01mol/L,则c(Ag+)2×c(CrO )>1×10-8,所以有沉淀生成,正确,答案选AD;
)>1×10-8,所以有沉淀生成,正确,答案选AD;
(5)常温下Ksp[Cr(OH)3]=10-32= c(OH-)3×c(Cr3+), c(Cr3+)降至10-5mol·L-1时,c(OH-)=1×10-9mol/L,则c(H+)=1×10-5mol/L,pH=5.
考点:考查元素推断,溶液浓度的计算,物质推断,离子浓度的比较,沉淀的溶解平衡的应用


科目:高中化学 来源: 题型:填空题
(14分)A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。
请回答下列问题。
(1)元素D在周期表中的位置 。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示) 。
(3)若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式: 。
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式: 。冶炼金属E时,用石墨做电极。E在(填“阴”或“阳”) 极得到,电解过程中,阳极石墨需要不断补充,结合电极反应说明其原因是 。
(5)由A、B、C三种元素以原子个数比4:2:3形成化合物X,X中所含化学键类型有 。土壤中含有X中的阳离子在硝化细菌的催化作用下被氧气氧化为其阴离子,写出其离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(16分)等电子原理的基本观点是:原子数相同且价电子总数相等的分子或离子具有相同的化学键类型和空间构型,互称为等电子体。等电子体的结构相似,物理性质相近。如:N2、CO与C22-、CN-为等电子体。
(1)已知CaC2为离子化合物,则CaC2的电子式为 。
(2)聚丙烯腈俗称人造羊毛,由丙烯腈分子CH2=CH—CN经聚合反应生成;则CH2=CH—CN中C原子的杂化方式为 ;分子中σ键和π键数之比为 。
(3)CO常与过渡金属原子M形成配合物M(CO)n ,其中满足中心原子价电子数与配位体提供电子总数之和为18,若M为Fe,则n= 。
(4)CO与N2的结构相似,分子中含有共价三键,可表示为C≡O ;下表是两者的键能数据(单位:kJ·mol-1)
| | C-O | C=O | C≡O |
| CO | 357.7 | 798.9 | 1071.9 |
| | N-N | N=N | N≡N |
| N2 | 154.8 | 418.4 | 941.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
【化学–选修3:物质结构与性质】(15分)
X、Y、Z、W四种元素原子序数依次增大且均小于36。 Z基态原子最外层电子数是其内层电子总数的3倍,Y基态原子是同周期元素中未成对电子数最多的原子,X分别与Y、Z元素组合均可形成10电子微粒, W基态原子有10个价电子。回答下列问题(以下问题均以推知元素符号作答):
(1)若 YX3与X2Z﹑YX2-与ZX-﹑Y3-与Z2-性质相似,请写出Mg(YX2)2在一定条件下分解的化学反应方程式
⑵已知0℃时X2Z的密度为a g/cm3,其晶胞中X2Z分子的空间排列方式与金刚石晶胞类似,相似的原因是 。两个X2Z分子间的最近距离为 pm(用a和NA表示)。 已知X2Y的升华热是51 kJ/mol,除氢键外,X2Z分子间还存在范德华力(11 kJ/mol),则X2Z晶体中氢键的“键能”是 kJ/mol。
⑶ WZ是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面。工业上常以W(YZ3)2·6X2Z和尿素[CO(NH2)2]为原料制备。
①W2+的基态核外电子排布式为 ,其核外电子有 种运动状态。
②尿素分子中碳原子的杂化方式为 ,1 mol尿素分子中含有的σ键数为 。
③YZ3-的空间构型 。
④WZ晶体的结构与NaCl相同,但天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种WZ晶体中就存在如图所示的缺陷:一个W2+空缺,另有两个W2+被两个W3+所取代。其结果晶体仍呈电中性,但化合物中W和Z的比值却发生了变化。经测定某样品中W3+与W2+的离子数之比为6∶91。若该晶体的化学式为WxZ,则x= 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(12分)【化学——物质结构与性质】
氮族元素包括N、P、As、Sb和Bi五种元素。
(1)下列关于氮族元素的说法正确的是 。
| A.N2可用于填充霓虹灯。其发光原理是电子从能量较低的轨道跃迁到能量较高的轨道,以光的形式释放能量 |
| B.P、Na、S三种元素的第一电离能由大到小的顺序是:P>S>Na |
| C.基态As原子中,电子占据的最高能级为4d |
| D.Bi原子中最外层有5个能量相同的电子 |
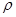 g·cm-3,晶胞的边长为acm,则阿伏加德罗常数为__ mol-l(用含ρ、a的式子表示)。
g·cm-3,晶胞的边长为acm,则阿伏加德罗常数为__ mol-l(用含ρ、a的式子表示)。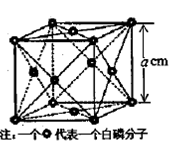
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(15分)下表中列出五种短周期元素X、Y、Z、W、T的信息。
| 元素 | 相关信息 |
| X | 基态原子最外层电子排布为nsnnpn+1 |
| Y | 其原子L层电子数是K层3倍 |
| Z | 其单质能与冷水剧烈反应,生成的阴阳离子电子数相同 |
| W | 其单质在Y2中燃烧,发出明亮的蓝紫色火焰 |
| T | 其最高正价与最低负价的代数和为6 |
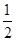 Y2(s)=Z2Y(s) △H1=-414KJ/mol
Y2(s)=Z2Y(s) △H1=-414KJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(12分)【化学——物质结构与性质】
(1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)和Fe(CO)x等。
①基态Fe3+的M层电子排布式为 ;
②尿素(H2NCONH2)分子中C原子的杂化方式是 ;
③配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x= 。
Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于 (填晶体类型)。
(2)下列说法正确的是 (填字母序号)。
| A.第一电离能大小:S>P>Si |
| B.电负性顺序:C<N<O<F |
| C.因为晶格能CaO比KCl高,所以KCl的熔点比CaO熔点低 |
| D.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高 |
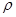 g·cm-3,阿伏加德罗常数为NA,求晶胞边长a= cm。(用含
g·cm-3,阿伏加德罗常数为NA,求晶胞边长a= cm。(用含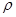 、NA的计算式表示)
、NA的计算式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
【物质结构与性质】
以氮化镓(GaN)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点。回答下列问题:
(1)镓为元素周期表第31号元素,镓原子价层电子排布图为___________。
(2)氮所在主族中第一电离能最大的元素是________(填元素符号,下同),镓所在主族中电负性最大的元素是____________________。
(3)传统的氮化镓制备方法是采用GaCl3与NH3在一定条件下反应,该反应的化学方程式为______________。
(4)氮化镓与金刚石具有相似的晶体结构,氮化镓中氮原子与镓原子之间以____相结合,氮化镓属于_______晶体。
(5)下图是氮化镓的晶胞模型:
①氮化镓中镓原子的杂化方式为__________,氮原子的配位数为___________。
②氮化镓为立方晶胞,氮化镓的密度为d g/cm3。列出计算氮化镓晶胞边长a的表达式:a=_______cm。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
I.用元素符号回答原子序数11-18的元素的有关问题:(填对应物质的化学式)
(1)最高价氧化物的水化物碱性最强的是 ;其电子式为:
(2)最高价氧化物的水化物呈两性的是 ;
(3)能形成气态氢化物且最稳定的是 ,其电子式为 .
II.化学是一门以实验为基础的自然科学,根据已有实验知识回答下列问题。
下列说法错误的是 。
| A.将Cl2通入紫色石蕊试液,溶液先变红后褪色 |
| B.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| C.配制1L0.5mol·L-1的NaCl溶液,需用托盘天秤称量29.25gNaCl固体 |
| D.常温下,可以用铁质容器储运浓硝酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com