
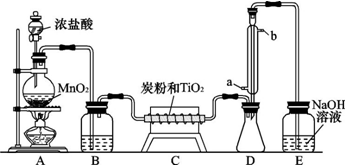
分析 装置A是利用二氧化锰和浓盐酸加热反应生成氯气的发生在,通过装置B中的浓硫酸干燥氯气,干燥的氯气通过装置C和碳、二氧化钛加热反应生成四氯化钛蒸气,进入装置D冷却,剩余的氯气最后用氢氧化钠溶液吸收,防止污染空气,
(1)装置中反应是二氧化锰和浓盐酸加热反应生成氯气的反应;
(2)根据制备的氯气中含有杂质水蒸气;
(3)由于TiO2、C、Cl2混合物在高温条件下制得TiCl4和一种有毒气体,根据化学反应中元素种类不变的规律可知:该有毒气体含有碳、氧两种元素,由碳、氧两种元素组成的有毒气体只有一氧化碳;因此TiO2、C、Cl2混合物在高温条件下反应生成TiCl4和一氧化碳;
(4)根据冷凝管内的水流方向由下向上,因为这样可以提高冷凝效果;四氯化钛沸点低,易挥发,所以要用冷凝管冷凝回收;
(5)E中氢氧化钠用于吸收氯气,防止污染空气;
(6)①根据TiCl4 遇空气中水蒸气发生水解;
②根据TiCl4 水解产生的氯化氢极易溶于水;
③根据氯气通过二氧化钛和炭粉的混合物得到的CO气体有毒.
解答 解:(1)装置中反应是二氧化锰和浓盐酸加热反应生成氯气的反应,反应的化学方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)因制备的氯气中含有杂质水蒸气,可用浓硫酸来除去,
故答案为:浓硫酸;干燥氯气;
(3)由于TiO2、C、Cl2混合物在高温条件下制得TiCl4和一种有毒气体,根据化学反应中元素种类不变的规律可知:该有毒气体含有碳、氧两种元素,由碳、氧两种元素组成的有毒气体只有一氧化碳;因此TiO2、C、Cl2混合物在高温条件下反应生成TiCl4和一氧化碳;
该反应的化学方程式为:TiO2+2Cl2+2C $\frac{\underline{\;650-850℃\;}}{\;}$TiCl4+2CO,
故答案为:TiO2+2Cl2+2C$\frac{\underline{\;650-850℃\;}}{\;}$ TiCl4+2CO;
(4)因根据冷凝管内的水流方向由下向上,即a进b出,因为这样可以提高冷凝效果;四氯化钛是无色液体,沸点为136℃较低,受热易挥发,所以冷凝管冷凝回收,故答案为:a;b;冷凝回流四氯化钛;
(5)E中氢氧化钠用于吸收氯气,防止污染空气,故答案为:吸收氯气;
(6)因氯气通过二氧化钛和炭粉的混合物得到的CO气体有毒,缺少CO的处理装置,所以由于CO气体有毒,缺少CO的处理装置.
故答案为:不能阻止E装置的水汽进入D装置,而引起四氯化钛水解;由于氯化氢和氯气易溶于氢氧化钠溶液,E装置会产生倒吸现象.
点评 本题考查物质的制备和性质探究,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及实验原理,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 18g H2O含有的氢原子数目为NA | |
| B. | 标准状况下,22.4L CO2含有的分子数目为NA | |
| C. | 1L1mol•L-1Na2SO4溶液中含有钠离子数目为NA | |
| D. | 1mol H2在Cl2中完全燃烧转移的电子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 闭合开关K后,电流计 指针不发生偏转,证明酒精溶液是非电解质 指针不发生偏转,证明酒精溶液是非电解质 | |
| B. | 闭合开关,往溶液中通入氯气,随着气体通入,电流计示数增大,故氯气是电解质 | |
| C. | 取用0.1 mol•L-1的蔗糖溶液替换酒精溶液,电流计的示数相同,说明蔗糖是非电解质 | |
| D. | 闭合开关,往烧杯中加NaCl固体,虽然固体溶解,由于不反应,故电流计指针不发生偏转 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2具有还原性,可用于漂白纸浆 | |
| B. | NH4HCO3受热易分解,可用作氮肥 | |
| C. | 氢氧化铝具有弱碱性,可用作净水剂 | |
| D. | 常温下铁能被浓硝酸钝化,可用铁质容器贮运浓硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
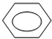 +HO-NO2→
+HO-NO2→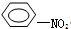 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com